第三章 酸碱反应和沉淀反应
人们对酸碱的认识经历了一个由浅入深,由低级到高级的认识过程。最初的直观认识:酸:有酸味,能使石蕊试液变红的,如食醋。碱:有涩味,滑腻感,能使红色石蕊变蓝,并能与酸反应生成盐和水,如小苏打。
1884年,瑞典化学家Arrhenius根据电解质化学理论,对酸碱作了以下定义:
酸:在水溶液中经电离只生成H+一种阳离子。
碱:在水溶液中经电离只生成OH-一种阴离子。
该定义使人类对酸碱的认识实现了从现象到本质的飞跃,但该定义也有局限性,它把酸和碱只限于水溶液。随着人们对酸碱认识的扩展。人们相继提出了溶剂理论,质子理论,电子理论和软硬酸碱的理论。本章将以酸碱质子理论为中心,讨论酸碱平衡问题。
酸:凡是能释放质子H+的任何含氢原子的分子或离子的物种,即质子的给予体。
碱:任何能与质子结合的分子或离子的物种。即质子的接受体。
![]()
![]()
可见,酸给出质子生成相应的碱,而碱结合质子后又生成相应的酸;酸与碱之间的这种依赖关系称共轭关系。相应的一对酸碱被称为共轭酸碱对。例如:HAc的共轭碱碱是Ac-,Ac-的共轭酸是HAc,HAc和Ac-是一对共轭酸碱。
既能给出质子,对能接受质子的物质为两性物质,例如:
HPO42-,H2PO42-,[Fe(OH)(H2O)5]2+,H2O等。
根据酸碱质子理论:酸碱解离反应是质子转移反应。
例如:HF在水溶液中的解离反应是由给出的质子的半反应和接受质子的半反应组成的。
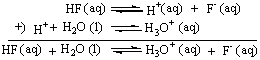
水是两性物质,它的自身解离反应也是质子转移反应。
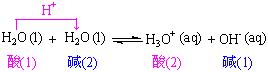
盐类水解反应也是离子酸碱的质子转移反应。例如:NaAc的分解:

NH4+的分解:
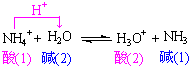
酸碱中和反应(包括非水溶剂中的反应)也是质子转移反应。
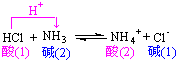
![]()
酸和碱的强度是指酸给出质子的能力和碱接受质子的能力的强弱。
在水溶液中:![]()
由此可以说明在水溶液中,HAc的酸性比HCN的酸性强。
区分效应:用一个溶剂把酸或碱的相对强弱区分开来,称为溶剂的“区分效应”。例如:H2O可以区分HAc、HCN酸性的强弱。
拉平效应:溶剂将酸或碱的强度拉平的作用,称为溶剂的“拉平效应”。水对强酸起不到区分作用,水能同等强度地将HClO4,HCl,HNO3等强酸的质子全部争取过来。
选取比水碱性弱的碱,如冰醋酸为溶剂对水中的强酸可体现出区分效应。例如上述强酸在冰醋酸中不完全解离,酸性强度依次为: HClO4>HCl>H2SO4>HNO3,所以H2O对以上强酸有拉平反应,冰醋酸对他们有区分效应。
结论:酸性越强,其共轭碱越弱;碱越强,其共轭酸越弱。
酸性:HClO4>H2SO4>H3PO4>HAc>H2CO3>NH4+>H2O
碱性:ClO4-<HSO4-<H2PO4-<Ac-<HCO3-<NH3<OH-
按照酸碱质子理论,水的自身解离平衡可表示为:
![]() 或
或![]()
标准平衡常数表达式:
![]()
或
![]()
![]() ——水的离子积常数,简称水的离子积。
——水的离子积常数,简称水的离子积。
25℃时,纯水中c(H+)=c(OH-)=1.0×10-7mol·L-1
![]() =1.0×10-14
=1.0×10-14
100℃时,纯水![]() =5.43×10-13
=5.43×10-13
可见,随着温度升高,水的![]() 增大。
增大。
溶液中H3O+浓度或OH-浓度的大小反映了溶液的的酸碱性的强弱。一般稀溶液中,c(H3O+)的浓度范围在(10-1~10-14)mol·L-1之间。在化学科学中,通常习惯于以c(H3O+)的负对数来表示其很小的数量级。
即pH=-{lgc(H3O+)};与pH对应的还有pOH,即pOH=-lg{c(OH-)}
在25℃时,
![]() =1.0×10-14
=1.0×10-14
![]() =14.00
=14.00
![]()
![]()
pH是用来表示水溶液酸碱性的一种标度。pH愈小,c(H3O+)愈大,溶液的酸性愈强。
通常所说的弱酸和弱碱是指酸、碱的基本存在形式为中性分子。它们大部分以分子形式存在于溶液中,只有少部分与水发生质子转移反应。只能给出一个质子的称为一元弱酸,能给出多个质子的为多元弱酸;只能接受一个质子的为一元弱碱,能接受多个质子为多元弱碱。
在一元弱酸HAc的水溶液中。存在着下列质子转移反应:
![]()
其平衡常数
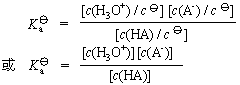
![]() —弱酸的HA的解离常数。弱酸的解离常数可以借助pH计测定溶液的pH来确定。若已知弱酸的解离常数
—弱酸的HA的解离常数。弱酸的解离常数可以借助pH计测定溶液的pH来确定。若已知弱酸的解离常数![]() ,就可以计算出一定浓度的弱酸的平衡组成。讲解例5-1。
,就可以计算出一定浓度的弱酸的平衡组成。讲解例5-1。
在弱酸、弱碱的解离平衡组成计算中常用到解离度(α)的概念,定义如下:
![]()
在定容反应中,解离度的表达式为:
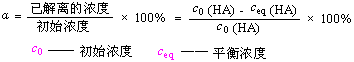
弱酸的解离度的大小也可以表示为酸的相对强弱。在温度和浓度相同的情况下,解离度大的酸,![]() 大,其pH小,为较强酸;解离度小的酸,
大,其pH小,为较强酸;解离度小的酸,![]() 小,其pH大,为较弱酸。
小,其pH大,为较弱酸。
稀释定律:在一定温度下(![]() 为定值),某弱电解质的解离度随着其溶液的稀释而增大。
为定值),某弱电解质的解离度随着其溶液的稀释而增大。
多元弱酸的解离,我们得出以下结论:
(1)多元弱酸的解离是分步进行的,一般![]() 溶液中的H+主要来自于弱酸的第一步电离,计算c(H3O+)或pH时可只考虑第一步电离。
溶液中的H+主要来自于弱酸的第一步电离,计算c(H3O+)或pH时可只考虑第一步电离。
(2)对于二元弱酸,当![]() 时,c(酸根离子)≈
时,c(酸根离子)≈![]() ,而与弱酸的初始浓度无关。
,而与弱酸的初始浓度无关。
(3)对于二元弱酸,若c(弱酸)一定时,c(酸根离子)与c(H3O+)成正比。
下面我们分别学习不同盐溶液的酸碱平衡:
1.强酸强碱盐(离子酸),例如,NH4Cl在水中全部解离:
![]()
Cl-(aq)不与水反应,而NH4+(aq)与H2O反应(水解反应)
![]()
该反应质子转移反应中,NH4+是质子酸,其解离常数为:
![]()
![]() 也叫NH4+的水解常数(也记作
也叫NH4+的水解常数(也记作![]() )
)
NH4+和NH3是共轭酸碱对。其实任何一对共轭酸碱的解离常数都符合这一关系,通式为:
![]()
两边分别取负对数:
![]()
25℃下,![]()
质子酸NH4+的解离度就是所谓的盐类的水解度。
![]()
![]()
由上分析可知,强酸弱碱盐的平衡问题,完全转化成了弱酸溶液的平衡问题。
2.弱酸强碱盐(离子碱):弱酸弱碱盐在水溶液中呈碱性,是因为弱酸根离子在水中发生水解的缘故。例如NaAc,溶于水完全解离。
![]()
Ac-发生水解反应(质子转移反应)
![]()
![]()
![]() ——质子碱Ac-的解离常数,也叫Ac-的水解常数(也记作
——质子碱Ac-的解离常数,也叫Ac-的水解常数(也记作![]() )。
)。
多元弱酸强碱盐的阴离子在水中的解离是分步进行的。如:Na3PO4的水解
![]()
![]()
![]()
![]()
![]()
![]()
![]() ,多元弱酸强碱盐问题就转化为多元弱碱的溶液平衡问题。
,多元弱酸强碱盐问题就转化为多元弱碱的溶液平衡问题。
多元酸的酸式盐,如:NaHCO3,NaH2PO4,Na2HPO4等,溶于水后完全解离生成的阴离子HCO3-,H2PO4-,HPO4-等既能给出质子又能接受质子,是两性,其水溶液既有碱性的,也有酸性的。
如何从理论上判断其酸碱性呢?例如:磷酸二氢钠NaH2PO4溶液中,H2PO4-的解离平衡:
![]()
![]()
H2PO4-的水解平衡:
![]()
![]()
解离大于水解,NaH2PO4溶液显酸性;相反,Na2HPO4溶液水解大于解离,显弱碱性。
4.弱酸弱碱盐:NH4Ac溶于水完全解离,解离出的NH4+,Ac-同时水解,存在下列平衡:
![]()
若![]() 溶液呈酸性NH4F
溶液呈酸性NH4F![]()
若![]() 溶液呈中性NH4Ac
溶液呈中性NH4Ac![]()
若![]() 溶液呈碱性NH4CN
溶液呈碱性NH4CN![]()
5.影响盐类水解的因素有盐的浓度、温度、溶液的酸碱度等。
盐的浓度:稀释有利于水解。
温度:加热有利于水解。盐类水解反应是中和反应的逆反应,因此是吸热反应,随着温度升高,
水解常数增大,水解加剧。
溶液的酸碱度:加酸抑制水解。例如:
![]()
![]()
![]()
配制这些盐的溶液时,通常先将盐溶于较浓的相应的酸中,然后再加水稀释到一定浓度。即利用改变酸度的方法,使水解达到平衡。
在HAc溶液中,存在下列平衡:![]()
向该溶液中加入与HAc含有相同离子的强电解质NH4Ac,c(Ac-)增加,上平衡向左移动,即HAc的解离度将减小。像这样在弱电解质溶液中,加入与其含有相同离子的易溶强电解质而使弱电解质的解离度降低的现象称为同离子效应。
前面已经计算出,0.10mol·L-1HAc溶液pH=2.89,α=1.3%。可见,HAc的解离度的确降低了很多。
首先,我们先分析下表的实验数据。
| 1.8×10-5mol·L-1HCl | 0.10mol·L-1HAc-0.10mol·L-1NaAc |
1.0L溶液的pH值 | 4.74 | 4.74 |
加0.010molNaOH(s)后 | 12.00 | 4.83 |
加0.010molHCl后 | 2.00 | 4.66 |
在稀盐酸中(1.8×10-5mol·L-1)溶液中,加入少量NaOH或HCl,pH有较明显的变化,说明这种溶液不具有保持pH相对稳定的性能。但在这对共轭酸碱组成的溶液中,加入少量的强酸或强碱,溶液的pH改变很小。这类溶液具有缓解改变氢离子浓度而保持pH基本不变的性能。
具有能保持pH相对稳定性能的溶剂,即不因加入少量强酸和强碱而显著改变的溶液叫缓冲溶液。
缓冲溶液中存在的质子转移反应为:![]()
![]()
溶液中HA、A-是大量的,H3O+是少量的,c(H3O+)取决于c(HA)/c(A-)。
当加入少量强碱,发生强碱与强酸的中和反应:![]()
c(A-)略有增加,c(HA)略有减少,但因溶液中HA、A-是大量的,c(HA)/c(A-)变化不大,因此溶液中c(H3O+)或pH基本不变。
当加入少量强酸,将发生如下中和反应:![]()
使溶液中c(A-)略有减少,c(HA)略有增加,但因溶液中HA、A-是大量的,c(HA)/c(A-)变化不大,因此溶液中c(H3O+)或pH基本不变。
由缓冲溶液原理可知:![]()
将等式两边分别取负对数:![]() 或
或![]()
对共轭酸碱来说,25℃时,![]() 、
、![]()
注意:c(HA)和c(A-)是共轭酸、碱的平衡浓度,但由于同离子效应的存在,除了![]() 的情况外,通常用初始浓度c0(HA)和c0(A-)代之。在各种酸碱溶液中,至少有一种酸(或碱)与溶剂水的解离反应同时存在,H+或OH-同时参与两(多)种解离平衡。在计算pH时要善于抓住主导反应,即依据生成cH+或cOH-大的解离平衡来计算系统的组成。此外,在计算弱酸,弱碱溶液的pH值时,只有溶液浓度不太稀(如大于10-4mol·L-1)时,才能不考虑水的解离平衡。
的情况外,通常用初始浓度c0(HA)和c0(A-)代之。在各种酸碱溶液中,至少有一种酸(或碱)与溶剂水的解离反应同时存在,H+或OH-同时参与两(多)种解离平衡。在计算pH时要善于抓住主导反应,即依据生成cH+或cOH-大的解离平衡来计算系统的组成。此外,在计算弱酸,弱碱溶液的pH值时,只有溶液浓度不太稀(如大于10-4mol·L-1)时,才能不考虑水的解离平衡。
提问学生思考:若由NaH2PO4与Na2HPO4构成缓冲系统,如何计算溶液的pH值?
提示:![]()
缓冲溶液的pH主要是由![]() 或
或![]() 决定的,还与c(A-)/c(HA)有关。当c(A-)/c(HA)=1/10~10/1时,缓冲作用有效,此范围叫做缓冲范围。缓冲溶液的缓冲能力是有限的。分析化学中定义:使缓冲溶液的pH值改变1.0所需的强酸或强碱的量,称为缓冲能力。当c(A-)/c(HA)接近1时,缓冲能力大。总之,要使缓冲有效,不仅应使缓冲溶液pH在溶液范围之内而且应尽可能接近
决定的,还与c(A-)/c(HA)有关。当c(A-)/c(HA)=1/10~10/1时,缓冲作用有效,此范围叫做缓冲范围。缓冲溶液的缓冲能力是有限的。分析化学中定义:使缓冲溶液的pH值改变1.0所需的强酸或强碱的量,称为缓冲能力。当c(A-)/c(HA)接近1时,缓冲能力大。总之,要使缓冲有效,不仅应使缓冲溶液pH在溶液范围之内而且应尽可能接近![]() 。此外,共轭酸碱的浓度应适当的大,才能保证较强的缓冲能力。
。此外,共轭酸碱的浓度应适当的大,才能保证较强的缓冲能力。
缓冲溶液的选择配制原则为:
(1)缓冲溶液除了参与和H+或OH-有关的反应外,不能与反应系统中的其他物质发生副反应。
(2)![]() 或
或![]() 尽可能接近所需溶液的pH。
尽可能接近所需溶液的pH。
小结:请同学们重点掌握一元弱酸(碱)的解离平衡及其平衡组成的计算,缓冲溶液pH值的计算。请通过课后习题的练习加以巩固所学知识点。
在上一节中,我们系统学习了水溶液中的酸碱平衡,这是一种均相反应。除此之外,另一类重要的离子反应是难溶电解质在水中的溶解,即在含有固体难溶电解质的饱和溶液中,存在着电解质与由它解离产生的离子之间的平衡,叫做沉淀溶解平衡。这是一种多相离子平衡。沉淀的生成和溶解现象在我们的周围经常发生。例如人体内肾结石的形成,就是难溶盐草酸钙和磷酸钙的生成;自然界中的钟乳石的形成,就是碳酸钙沉淀的生成和溶解反应有关;工业上,可以用碳酸钠和消石灰制取烧碱等。这些实例说明,沉淀-溶解平衡对生物化学、医学、工业生产等有着深远影响,可以提供理论指导。
溶解性是物质重要的性质之一,常以溶解度来定量标明物质的溶解度。在一定温度下,达到溶解平衡时,一定的溶剂中含有溶质的质量,叫作溶解度,通常以符号S表示。对于水溶液来说,通常以饱和溶液中每100g水所含溶质的质量来表示,即:以"g/100g水"表示。许多无机化合物在水中溶解时,能形成水合阳离子和阴离子,称其为电解质,电解质的溶解度有很大的差异,一般分为可溶、微溶和难溶等不容的等级。
在一定温度下,将难溶电解质晶体放入水中,就发生溶解和沉淀两个过程。当溶解和沉淀速率相等时,便建立了一种动态的多相平衡。以BaSO4晶体溶于水形成水合离子的过程为例,可表示为:
![]()
平衡常数为:![]()
![]() 叫做溶度积常数,简称溶度积。
叫做溶度积常数,简称溶度积。
对于一般的沉淀反应:![]()
溶度积常数的通式:![]()
即,溶度积等于沉淀-溶解平衡时离子浓度幂的乘积,每种离子浓度的幂与化学计量式中的计量数相等。要特别注意:KspӨ�������的数值在稀溶液中不受其他离子的存在的影响,只取决于温度。温度升高,多数难溶化合物的溶度积增大。
溶度积和溶解度都可以用来表示难溶电解质的溶解性。两者既有联系,又有区别。在相关溶度积的计算中,离子浓度必须是物质的量浓度,其单位是mol·L-1,而溶解度的单位往往是g/100g水。因此,计算时有时要先将难溶电解质的溶解度S的单位换算mol·L-1。
![]()
平衡浓度/mol·L-1 nS mS
![]()
对于AB型:![]()
对于AB2型:![]()
难溶电解质的沉淀-溶解平衡与其他动态平衡一样,完全遵循Le Chatelier原理。对于难溶电解质的多相离子平衡物质:反应商J={c(Am+)}n{c(Bn-)}m沉淀-溶解平衡的反应商判据,(反应商又被称为难溶电解质的离子积)即溶度积规则:
![]() ,平衡向左移动,沉淀析出;
,平衡向左移动,沉淀析出;
![]() ,处于平衡状态,饱和溶液;
,处于平衡状态,饱和溶液;
![]() ,平衡向右移动,无沉淀析出,若原来有沉淀存在,则沉淀溶解。
,平衡向右移动,无沉淀析出,若原来有沉淀存在,则沉淀溶解。
在难溶电解质饱和溶液中,加入含有相同离子的易溶强电解质,而使难溶电解质的溶解度降低的作用称为同离子效应。这与上一章在缓冲液那一节所学的弱酸或弱碱的同离子效应也是一直的。
在实验中,常常利用加入适当过量的沉淀剂,使沉淀趋于完全。但是注意,如果加入沉淀剂太多时,不仅不会产生明显的同离子效应,往往还会产生相反的作用,使沉淀的溶解度增大,这种影响之一就是盐效应。
观察表6-2,AgCl在KNO3溶液中的溶解度(25℃)。可见,AgCl在KNO3溶液中的溶解度比其它纯水中的溶解度大,并且KNO3的浓度越大,AgCl溶解度也越大。 这种由于加入易溶强电解质而使难溶电解质溶解度增大的效应,叫做盐效应。 注意:加入具有相同离子的电解质,在产生同离子效应的同时,也能产生盐效应。
分析表6-3,PbSO4在Na2SO4溶液中的溶解度:当Na2SO4的浓度从0增加到0.04mol·L-1时,PbSO4溶解度逐渐变小,同离子效应起主导作用,当Na2SO4的浓度大为0.04mol·L-1时,PbSO4的溶解度最小;当Na2SO4的浓度大于0.04mol·L-1时,PbSO4的溶解度逐渐增大,盐效应起主导作用。一般说来,若难溶电解质的溶度积很小时,盐效应的影响很小,可忽略不计;若难溶电解质的溶度积较大时,溶液中各种离子的总浓度也较大时,就应该考虑盐效应的影响。
如果难溶电解质MA的阴离子是某弱酸的共轭碱,由于共轭碱对质子有较强的亲和能力,则它们的溶解度将随pH的减小而增大。这类难溶电解质就是通常所说的难溶弱酸盐和难溶金属氢氧化物。氢氧根离子是水中的最强碱,它是弱酸水的共轭碱,从这个意义上说,金属氢氧化物也是弱酸盐。利用弱酸盐在酸中溶解度的差异,我们可以通过控制溶液的pH来达到分离金属离子的目的。
1.难溶金属氢氧化物溶于酸,沉淀溶解平衡:
![]()
![]()
利用上式可以计算氢氧化物开始沉淀和沉淀完全时溶液的c(OH-),从而求出相应条件的pH值。
开始沉淀时:
![]()
c0(Mn+)----溶液中Mn+离子的起始浓度
即溶液中氢氧根离子的浓度小于c始(OH-),就不形成Mn(OH)n沉淀;若溶液中有沉淀,只要将溶液的氢氧根离子控制在c始(OH-)以下,原有的M(OH)n沉淀将溶解,且溶解后溶液中Mn+离子浓度为c0(Mn+)。
沉淀完全时:
![]()
分析化学中认为,当溶液中离子浓度小于1.0×10-5mol·L-1时,认为这种离子已沉淀完全。利用不同离子形成氢氧化物沉淀和沉淀完全时溶液的pH值的差异,可将不同的离子进行分离。
一些两性氢氧化物,既可以溶于酸,又可以溶于碱,那溶液pH值在一定区间内,化合物是以氢氧化物沉淀存在的。例如:
![]()
![]()
pH在4~11范围内Al(OH)3基本不溶解。对于KspӨ�������不是很小(KspӨ�������:10-12~10-13)的难溶金属氢氧化物,常使用氨-铵盐缓冲溶液来控制pH值,达到沉淀的生成或溶解的目的。
金属硫化物:很多金属硫化物在水中都是难溶的,而且它们的溶度积常数彼此有一定的差异,并各有特定的颜色。在实际应用中,常利用硫化物溶度积的差异以及硫化物的特征颜色,来分离或鉴定某些金属离子。最近研究表明,S2-像O2-一样是很强的弱碱,在水中不能存在。析出难溶金属硫化物MS的多相离子平衡不能写作:
MS(s)![]() M2+(aq)+S2-(aq)
M2+(aq)+S2-(aq)
必须考虑强碱S2-对质子的亲和作用,
S2-(aq)+H2O(l)![]() HS-(aq)+OH-(aq)
HS-(aq)+OH-(aq)
所以,难溶金属硫化物的多相离子平衡应写作:
MS(s)+H2O(l)![]() M2+(aq)+OH-(aq)+HS-(aq)
M2+(aq)+OH-(aq)+HS-(aq)
Ky={c(M2+)}{c(OH-)}{c(HS-)}
而难溶金属硫化物在酸中的沉淀-溶解平衡为:
MS(s)+2H+(aq)![]() M2+(aq)+H2S(aq)
M2+(aq)+H2S(aq)
![]()
或![]()
![]() -难溶金属硫化物在酸中的溶度积常数。
-难溶金属硫化物在酸中的溶度积常数。
许多难溶化合物在配位剂的作用下,能够生成配离子而溶解。例如:
![]()
![]()
![]()
一般情况下,当难溶化合物的溶度积不很小,并且配合物的生成常数比较大时,就有利于配位溶解反应的发生。此外,配位剂的浓度也是影响难溶化合物能否发生配位溶解的重要因素之一。
前面我们讨论的都是加一种试剂只能使一种离子生成沉淀的情况。实际上,溶液中往往含有多种可被沉淀的离子,即当加入某种沉淀试剂的时候,可能分别和溶液中多种离子发生反应而产生沉淀。在这种情况下,当溶液中存在多种可被沉淀的离子时,加入沉淀剂会产生怎样的结果呢?是同时沉淀下来呢?还是一步一步地按先后次序沉淀呢?
在Na2S和K2CrO4等比例混合的溶液中,加入Pb(NO3)2溶液,先生成黑色的PbS沉淀,后生成黄色的PbCrO4沉淀。另外,在含有相同浓度(1×10-3mol·L-1)的Ag+和Pb2+的混合溶液中,先加一滴0.1mol·L-1的K2CrO4溶液,此时只有黄色的PbCrO4沉淀析出;如果继续滴加溶液,才有砖红色的Ag2CrO4沉淀析出。这种先后沉淀的现象,叫做分步沉淀或分级沉淀。掌握了分步沉淀的规律,就可根据具体情况,适当的控制条件,达到分离离子的目的。
有些沉淀既不溶于水也不溶于酸,还无法用配位溶解和氧化还原溶解的方法把它直接溶解。这时,可把一种难溶电解质转化为另一种难溶电解质,然后使其溶解。这种把一种沉淀转化为另一种沉淀的过程,叫做沉淀转化。如在AgNO3和K2CrO4的混合溶液中,再逐滴加入NaCl溶液,边加边振荡,沉淀由红变白。
小结,在本章中,我们继续学习了关于平衡的讨论,该内容与酸碱平衡有很多相似之处,我们在课堂上就讲的没那么详细,请同学们课后把平衡相关内容联系起来,思考其想通之处,而不是分开死记硬背。
1 / 11