第十一章 卤素和氧族元素
p区元素概述
1. 各族元素性质由上到下的变化规律出现突变
2. 多种氧化态(因为价电子构型为ns2np1-5)
3. 电负性大,形成共价化合物
突变:
1. 第一排元素反常性:(只有2s,2p轨道) 形成配合物时,配位数最多不超过4
第一排元素单键键能小于第二排元素单键键能
E(N-N)=159 kJ×mol-1 E(O-O)=142 kJ×mol-1 E(F-F)=158 kJ×mol-1
E(P-P)=209 kJ×mol-1 E(S-S)=264 kJ×mol-1 E(Cl-Cl)=244 kJ×mol-1
2. 中间排元素异样性(d区插入) 例如:溴酸、高溴酸氧化性均比其它卤酸、高卤酸强。
3. 最后三个元素性质缓慢地递变(镧系收缩)。
多种氧化态:
因为价电子构型为:ns2np1-5,p区元素有多个价电子,所以可以形成多种氧化态。
例如:氯有+1,+3,+5,+7,-1,0等氧化态。
对于同族元素而言从上到下,随着原子序数的增加低氧化态化合物比高氧化态化合物稳定,这种现象称为惰性电子对效应。
例:Sn(II)<Sn(IV) Pb(II)>Pb(IV)
§11.2 卤素
卤素是元素周期系第ⅦA族元素,包括氟、氯、溴、碘、砹。
卤族元素的性质变化如下:
卤素元素符号 F Cl Br I
价电子构型 2s22p5 3s23p5 4s24p5 5s25p5
公价半径/pm 66 99 114 133
电负性 3.98 3.16 2.96 2.66
电离能/(kJ·mol-1) 1687 1257 1146 1015
11.2.2 卤素单质
⒈卤素单质的物理性质

⒉卤素单质的化学性质
卤素是很活泼的非金属元素。卤素单质具有很强的氧化性,能与大多数元素直接化合。
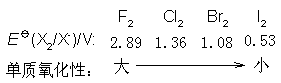
例如:位于前面的卤素单质可以氧化后面卤素的阴离子。
Cl2 + 2Br- → 2Cl- + Br2
★ 卤素与水反应分为两类:
氧化反应: 2X2 + 2H2O → 4X- + 4H+ + O2
激烈程度:F2>Cl2>Br2,碘不发生此类反应。
歧化反应: ![]()
![]()
![]()
![]()
可见,反应进行的程度Cl2>Br2>I2,氟只发生第一类反应。通常所用的氯水、溴水、碘水主要成分是单质。
★ 卤素在碱性条件下发生两类歧化反应: X2 + 2OH- → X- + XO- + H2O
3X2 + 6OH- → 5X- + XO3- + 3H2O
不同元素单质发生歧化反应的条件及主要产物见下表:
常温 加热 低温
Cl2 ClO- ClO3- ClO- pH>4
Br2 BrO3- BrO3- BrO-(0℃) pH>6
I2 IO3- IO3- IO3 pH>9
11.2.3 卤素的氢化物
⒈卤素的氢化物概述
卤素的氢化物称为卤化氢,即氟化氢HF、氯化氢HCl、溴化氢HBr、碘化氢HI等。常温下卤化氢都是无色、有刺激性气味的气体。卤化氢易溶于水,其水溶液叫氢卤酸。除氟化氢外,其它氢化物均为强酸。
⒉氯化氢和盐酸
制备: 直接合成法: ![]()
复分解反应:
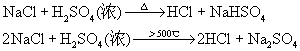
纯盐酸为无色溶液,有氯化氢的刺激性气味。一般浓盐酸的浓度约为39%,相当于12mol·l-1,密度为1.19g·cm-3。工业用的盐酸为30%左右,由于带有杂质而带黄色。
用途:盐酸是重要的化工生产原料,常用来制备金属氯化物、苯胺和染料等产品。盐酸在冶金工业、石油工业、印染工业、皮革工业、食品工业及轧钢、焊接、电镀、搪瓷、药物等部门也有广泛的应用。
⒊氟、溴、碘的氢化物
氟化氢的制备
一般用复分解反应法:
CaF2 + H2SO4(浓) → CaSO4 + 2HF
氟化氢是无色、有刺激性气味并具有强烈腐蚀性的有毒气体,当皮肤接触HF时会引起不易痊愈的灼伤;氢氟酸的蒸汽对皮肤也有同样的危害,因此,使用氢氟酸时应特别注意安全。氟化氢和氢氟酸都能和二氧化硅作用,生成挥发性的四氟化硅:
SiO2 + 4HF → SiF4 + 2H2O
二氧化硅是玻璃的主要成分,氢氟酸能腐蚀玻璃。因此,常用塑料容器来贮存氢氟酸。
氢氟酸可以用来刻蚀玻璃或溶解各种硅酸盐。
溴化氢和碘化氢的制备
一般用卤化物水解法: PBr3 + 3H2O → H3PO3 + 3HBr
PI3 + 3H3O → H3PO3 + 3HI
也可直接用水和卤素与磷混合物反应制备卤化氢。
2P + 3Br2 + 6H2O → 2H3PO3 + 6HBr
2P + 3I2 + 6H2O → 2H3PO3 + 6HI
溴化氢和碘化氢的制备不能用单质直接合成法,因溴和碘与氢反应速度缓慢、产率低而不适合。溴化氢和碘化氢的制备也不能用卤化物与浓硫酸的复分解反应来制备,因为HBr、HI有显著的还原性,它们将与浓硫酸进一步发生氧化还原反应:
2HBr + H2SO4(浓) → Br2 + SO2 + 2H2O
8HI + H2SO4(浓) → 4I2 + H2S + 4H2O
所以,实际上得不到纯的溴化氢和碘化氢。如果改用无氧化性的高沸点酸浓磷酸代替浓硫酸,可以制得溴化氢和碘化氢。
⒋ 卤化氢性质的比较

11.2.4 卤化物和多卤化物
⒈卤化物
卤素和电负性比它小的元素生成的化合物叫卤化物。卤化物可以分为金属卤化物和非金属卤化物,根据卤化物的键型,又可以分为离子型卤化物和共价型卤化物。
⑴金属卤化物
所有金属都能形成卤化物。碱金属、碱土金属以及镧系、锕系元素的卤化物大多数属于离子型或接近离子型,例如:NaX,BaCl2,LaCl3等。当阴阳离子极化作用比较明显时,表现出一定的共价性,如:AgCl等。有些高氧化值的金属卤化物则为共价型卤化物,如,AlCl3,SnCl4,FeCl3,TiCl4等。
不同类型卤化物,性质上存在差异,见下表:
卤化物类型 离子型 共价型
熔点 高 低
溶解性 大多易溶于水 易溶于有机溶剂
导电性 水溶液、熔融导电 无导电性
在金属卤化物中,对应氢氧化物不是强碱的都易水解,产物为氢氧化物或碱式盐。需特殊记忆的有:
SnCl2 + H2O → Sn(OH)Cl + HCl
SbCl3 + H2O → SnOCl + 2HCl
BiCl3 + H2O → BiOCl + 2HCl
⑵非金属卤化物
非金属硼、碳、硅、氮、磷等都能与卤素形成各种相应的卤化物。这些卤化物都是共价型的。
非金属卤化物水解产物一般为两种酸,例如:BX3,SiX4,PCl3等。
⒉多卤化物
有些金属卤化物能与卤素单质或卤素互化物发生加合作用,生成的化合物称为多卤化物。例如:KI3,KICl2,KI2Cl,KIBrCl等。
含有3个卤原子的多卤化物阴离子的空间构型几乎都是直线型的。如卤原子不同时,则半径较大的卤原子位于中间,而半径较小的卤原子位于两侧。
I2在含有I-的溶液中溶解度比在纯水中溶解度大得多,与生成多卤化物有关,即发生如下加合反应:
KI + I2 → KI3
11.2.5 卤素的含氧化合物
⒈卤素的含氧化合物概述
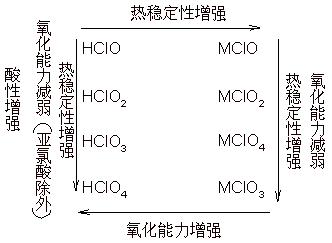
卤素的含氧化合物有氧化物、氢氧化物(含氧酸)、含氧酸盐,其稳定性依次增强。
⒉各类卤素含氧酸根的结构
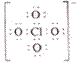
对于任何类型的卤素含氧酸根, ![]() ,价层电子对的空间构型为四面体构型,即卤原子X都采用sp3杂化,卤原子用sp3杂化轨道与氧原子O成键。
,价层电子对的空间构型为四面体构型,即卤原子X都采用sp3杂化,卤原子用sp3杂化轨道与氧原子O成键。
![]()
![]()
![]()
![]()
卤原子氧化值 +1 +3 +5 +7
名称 次卤酸根 亚卤酸根 卤酸根 高卤酸根
离子空间构型 直线型 V字型 三角锥 四面体
空间构型

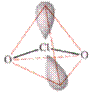
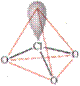
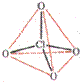
模型 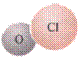
![]()

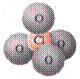
电子结构式 ![]()
![]()
![]()
⒊次卤酸及其盐
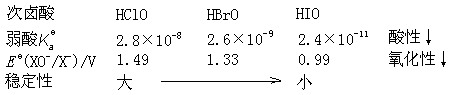
次氯酸很不稳定,只能存在于稀溶液中,而不能制得浓酸。次氯酸见光受热均不稳定。
![]()
![]()
次溴酸、次碘酸稳定性更差。
次氯酸是很强的氧化剂。氯气的漂白作用就是由于它与水作用而生成次氯酸的缘故,所以完全干燥的氯气没有漂白作用。
把氯气通入冷的碱溶液中,便生成次氯酸盐。
Cl2 + NaOH → NaClO + NaCl + H2O
漂白粉是用氯气与消石灰作用而制得的,是次氯酸钙、氯化钙和氢氧化钙的混合物。
2Cl2 + 3Ca(OH)2 → Ca(ClO)2 + CaCl2·Ca(OH)2·H2O + H2O
溴和冷的碱溶液作用能生成次溴酸盐。NaBrO在分析化学上常用作氧化剂。次碘酸的稳定性极差,所以,碘与碱溶液反应得不到次碘酸盐。
*⒋亚卤酸及其盐
目前已获得的亚卤酸及其盐是亚氯酸及其盐。反应为:
2ClO2 + H2O → HClO2 + HClO3
Ba(ClO)2 + H2SO4 → 2HClO2 + BaSO4
二氧化氯与过氧化物反应时,可得到亚氯酸盐和氧。
2ClO2 + Na2O2 → 2NaClO2 + O2
2ClO2 + BaO2 → Ba(ClO2)2 + O2
亚氯酸盐虽比亚氯酸稳定,但加热或敲击固体亚氯酸盐时,立即发生爆炸,分解成为氯酸盐和氧化物。亚氯酸盐的水溶液较稳定,具有强氧化性,可作漂白剂。
⒌卤酸及其盐

氯酸是强酸,仅存在于水溶液中。氯酸也是强氧化剂,例如
2HClO3 + I2 → 2HIO3 + Cl2
HClO3 + 5HCl → 3Cl2 + 2H2O
重要的氯酸盐有氯酸钾和氯酸钠。KClO3受热分解,因条件不同而产物不同。
![]()
4KClO3→3KClO4+KCl]
固体氯酸钾KClO3是强氧化剂,与各种易燃物混合后,经撞击会引起爆炸起火。因此,KClO3多用来制造火柴和焰火等。
KClO3和C11H22O11混合物的火焰 KClO3—火柴头中的氧化剂
常用氯酸钡与稀硫酸作用制取氯酸: Ba(ClO3)2 + H2SO4 → BaSO4 + 2HClO3
溴酸和碘酸的制备,通常用选择适当的氧化剂而获得。例如:
Br2 + 5Cl2 + 6H2O→ 2HBrO3 + 10HCl
I2 + 5Cl2 + 6H2O→ 2HIO3 + 10HCl
3I2 + 10HNO3 → 6HIO3 + 10NO + 2H2O
⒍高卤酸及其盐
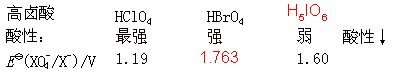
高卤酸都是强氧化剂,均已获得纯物质,稳定性好。例如:
![]()
高氯酸是最强的无机含氧酸。无水的高氯酸是无色液体。HClO4的稀溶液比较稳定,但浓HClO4不稳定,受热分解。
4HClO4 → 2Cl2 + 7O2 + 2H2O
浓HClO4是强氧化剂,与有机物接触会引起爆炸,所以贮存时必须远离还原性物质。务必注意安全!高氯酸在钢铁分析中常用来溶解矿样。
高氯酸的盐多易溶于水,但K+, ![]() ,Cs+,Rb+的高氯酸盐溶解度都很小。有些高氯酸盐易吸湿,如Mg(ClO4)2和Ba(ClO4)2可作干燥剂。KClO4常用作制造炸药。NH4ClO4是现代火箭推进剂的主要成分。
,Cs+,Rb+的高氯酸盐溶解度都很小。有些高氯酸盐易吸湿,如Mg(ClO4)2和Ba(ClO4)2可作干燥剂。KClO4常用作制造炸药。NH4ClO4是现代火箭推进剂的主要成分。
⒎氯的各种含氧酸及其盐的性质的一般规律
§11.3 氧族元素
11.3.1 氧族元素概述
氧族元素是周期系第ⅥA族元素,包括氧(O)、硫(S)、硒(Se)、碲(Te)、钋(Po)五种元素,其价电子构型为:ns2np4。
元素符号 | O | S | Se | Te | Po |
单质性质 | 典型非金属 | 准金属 | 放射性金属 | ||
存在形式 | 单质或矿物 | 共生于重金属的硫化物中 | |||
单质化学活性 | 由大到小 | ||||
本节的讨论重点是氧、硫及其化合物。硒、碲的单质见下图:
![]()
![]()
11.3.2 氧及其化合物
⒈氧
氧是地壳中分布最广泛的元素,其丰度居各种元素之首,其质量约占地壳的一半。在海洋中氧以水的形式存在,在大气中氧以单质状态存在,在岩石和土壤中氧以硅酸盐、氧化物及其它含氧阴离子的形式存在。
氧的电子排布式为: ![]()
其结构式为: ![]() ,具有顺磁性。
,具有顺磁性。
常温下氧气只能将某些还原性的物质(如NO,SnCl2,H2SO3等)氧化。在加热条件下,除卤素、少数贵金属(如Ag、Pt等)以及稀有气体外,氧气几乎能与所有元素直接化合成相应的氧化物。
⒉臭氧
臭氧O3是氧气O2的同素异形体。臭氧在地面附近的大气层中含量极少,而在大气层的最上层,由于太阳对大气中的氧气的强烈辐射作用,形成了一层臭氧层。臭氧层能吸收太阳光的紫外辐射,成为保护地球上生命免受太阳将辐射的天然屏障。
 臭氧分子的构型为V型,如图所示:
臭氧分子的构型为V型,如图所示:
中心氧原子以2个sp2杂化轨道与另外两个氧原子形成σ键,第三个sp2杂化轨道被孤对电子所占有。此外,中心氧原子的未参与杂化的p轨道上有一对孤对电子,两端的氧原子与其平行的p轨道上各有一个电子,它们之间形成垂直于分子平面的三中心四电子大π键,用 ![]() 表示。
表示。
臭氧分子中键角为117°,分子的偶极矩μ=1.8×10-3c·m。臭氧是唯一的极性单质。
臭氧是淡蓝色的气体,有鱼腥味。臭氧极不稳定,在常温下缓慢分解:
O3(g) → 3O2(g)
二氧化锰的存在可加速臭氧的分解。臭氧的另一个重要性质就是它的强氧化性,例如:
O3 + 2I- + 2H+ → I2 + O2 + H2O
这个反应用于测定臭氧的含量。
利用臭氧氧化性和不易导致二次污染的优点,臭氧可用作消毒剂,用来净化废气、废水。
⒊过氧化氢
过氧化氢H2O2的分子结构:H2O2的分子结构如图所示,在H2O2的分子中有一个过氧键─O─O─,两个氧原子都以sp3杂化轨道成键,除相互连接成O─O键外,还各与一个氢原子相连。
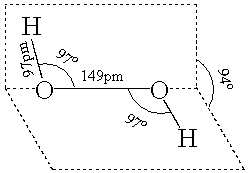
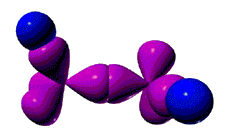
H2O2的性质:高纯度的H2O2在低温下比较稳定,分解作用比较平稳。当加热到426K以上,发生爆炸性分解:
2H2O2(l) → 2H2O + O2(g)
因此,H2O2应贮存在棕色瓶中,置于阴凉处。
H2O2具有弱酸性和氧化还原性。例如:
弱酸性: H2O2 + Ba(OH)2 → BaO2 + 2H2O
强氧化性: | 酸性条件:2Fe2+ + H2O2 + 2H+ → 2Fe3+ + 2H2O |
碱性条件:2[Cr(OH)4]- + 3H2O2 + 2OH- → 2[CrO4]2- + 8H2O |
过氧化氢还可将黑色的PbS氧化为白色的PbSO4:
PbS + 4H2O2 → PbSO4 + 4H2O
只有当H2O2与强氧化剂作用时才显示出其还原性。
2KMnO4 + 5H2O2 + 3H2SO4 → 2MnSO4 + 5O2 + K2SO4 + 8H2O
H2O2 + Cl2 → 2HCl + O2
过氧化氢也是一种不造成二次污染的氧化剂,所以常用作杀菌剂、漂白剂等。注意:浓度稍大的双氧水会灼伤皮肤,使用时应格外小心!
11.3.3 硫及其化合物
⒈单质硫
单质硫俗称硫磺,是分子晶体,很松脆,不溶于水。硫有几种同素异形体,斜方硫(菱形硫)、单斜硫、弹性硫等。天然硫一般是斜方硫。
| 斜方硫 | 单斜硫 | 弹性硫 |
密度/g·cm-1 | 2.06 | 1.99 |
|
颜色 | 黄色 | 浅黄 |
|
稳定条件 | <94.5℃ | 94.5℃~115℃ | 190℃的熔融硫用冷水速冷 |
外观 |
|
|
|

斜方硫和单质硫的分子都是由8个硫原子组成的环状结构,像皇冠一样,如图所示。在S8分子中,每个硫原子各以sp3杂化轨道中的两个轨道与相邻的两个硫原子形成σ键,而sp3杂化轨道中的另两个则各有一对孤对电子。单质硫与斜方硫的不同在于四面体中S8分子排列不同。
![]() 单质硫是分子晶体,熔点低,不溶于水而易溶于二硫化碳,四氯化碳等非极性溶剂。
单质硫是分子晶体,熔点低,不溶于水而易溶于二硫化碳,四氯化碳等非极性溶剂。
单质硫加热熔化后,温度升至160℃,S8环开始断开,并聚合成中长链大分子,因而液体颜色变暗,粘度显著增大。当温度达到190℃左右,倒入冷水中迅速冷却,可以得到弹性硫。此时,由于骤冷,长链状硫分子来不及成环,仍以绞结的长链存在于固体中,因而固体具有弹性。
硫的化学性质比较活泼,能与许多金属直接化合成相应的硫化物,也能与氢、氧、卤素(除碘外)、碳磷等直接作用生成相应的共价化合物。
硫与氧化性酸的作用: | S + 2HNO3 → H2SO4 + 2NO(g) |
S + 2H2SO4(浓) → 3SO2(g) + 2H2 | |
硫在碱中的歧化: |
|
|
⒉硫化氢和硫化物
⑴硫化氢
硫化氢H2S分子的构型与水分子相似,也呈"V"字形,当其分子极性比H2O弱。
通常用金属硫化物和非氧化性酸制备硫化氢:
FeS + 2HCl → H2S + FeCl2
也可用硫代乙酰胺水溶液加热水解的方法制取。
CH3CSNH2 + 2H2O → CH3COONH4 + H2S
硫化氢是无色有腐蛋味的剧毒气体。H2S中毒是由于它能与血红素中Fe2+作用生成FeS沉淀,因而使Fe2+失去原来正常的生理作用。硫化氢微溶于水,其水溶液为二元弱酸。
硫化氢最重要的性质就是它的强还原性。
★ 被空气氧化
![]()
![]()
所以硫化氢水溶液在空气中放置会逐渐变混浊。
★ 与中等强度氧化剂作用
H2S + 2Fe3+ → S + 3Fe2+ + 2H+ (注意:反应不生成Fe2S3或FeS)
H2S + X2 → S + 2X- + 2H+ (X=Cl,Br,I)
★ 与强度氧化剂反应
![]()
![]()
⑵金属硫化物
颜色:金属硫化物大多数为黑色,少数需特殊记忆。例如:SnS棕色,SnS2黄色,As2S3黄色,As2S5黄色,Sb2S3橙色,As2S5橙色,MnS肉色,ZnS白色,CdS黄色。
水解性:金属硫化物无论是微溶还是易溶,都会发生水解反应,即使是难溶金属硫化物,其溶解部分也
会发生水解。例如:Na2S、(NH4S)水溶液因水解而呈碱性;Cr2S3、Al2S3遇水发生强烈水解:
2M3+ + 3S2- + 6H2O → 2M(OH)3 + 3H2S (M=Al,Cr)
溶解性: ![]() 和碱金属硫化物及BaS易溶于水,其他碱土金属硫化物微溶于水(BeS难溶)。除此之外,大多数金属硫化物难溶于水。难溶于水的金属硫化物在不同的酸、碱中溶解程度也有差异,利用这些差异我们可将金属离子进行分离。
和碱金属硫化物及BaS易溶于水,其他碱土金属硫化物微溶于水(BeS难溶)。除此之外,大多数金属硫化物难溶于水。难溶于水的金属硫化物在不同的酸、碱中溶解程度也有差异,利用这些差异我们可将金属离子进行分离。
★ 稀酸溶解性硫化物:MnS、FeS、CoS、NiS、ZnS。
MS + 2H+ → M2+ + H2S(g)
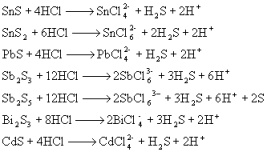
★ 浓盐酸配位溶解
★ 硝酸氧化溶解:
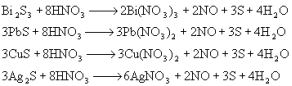
★ 王水溶解:
![]()
★ 碱溶(用NaOH或Na2S)

★ 氧化碱溶(Na2S2)
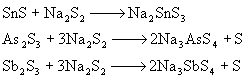
⒊多硫化物
在可溶性硫化物的溶液中加入硫粉时,硫溶解而生成相应的多硫化物,例如:
(NH4)2S + (x-1)S → (NH4)2Sx
随着硫原子数目x的增加,溶液颜色由黄→橙红→红。所以通常所得的多硫化物是含有不同数目硫原子的各种多硫化物的混合物。
多硫离子 ![]() 具有链式结构:
具有链式结构: ![]()
当x=2时,多硫化物称为过硫化物(同过氧化物)。
过硫化氢H2S2与过氧化氢的结构相似。
多硫化物的重要性质:
★ 遇酸不稳定
![]()
★ 还原性(次要)
3FeS2 + 8O2 → Fe3O4 + 6SO3
★ 氧化性(主要)
![]()
所以多硫化物用作厚皮的除毛剂,果木、棉花的杀虫剂。
⒋二氧化硫、亚硫酸及其盐
二氧化硫制备:工业上利用焙烧硫化物矿制取SO2:
3FeS2 + 8O2 → Fe3O4 + 6SO2
实验室中常用亚硫酸盐与酸作用制取少量二氧化硫,也可用浓硫酸与铜共热制取二氧化硫。
二氧化硫的结构:气态的SO2的分子构型为V形,如图所示。SO2分子中,硫原子以两个sp2杂化轨道分别与两个氧原子形成σ键,而另一个sp2杂化轨道上则保留1对孤对电子,硫原子的未参与杂化的p轨道上的2个电子与两个氧原子的未成对p电子形成三中心四电子大π 键
键 ![]() 。
。
二氧化硫和亚硫酸的性质:SO2是无色、具有强烈刺激性气味的气体。液态SO2能构解离,是一种良好的非水溶剂。
![]()
SO2的汽化焓很大,液态SO2可用作制冷剂。
SO2易溶于水,生成很不稳定的亚硫酸H2SO3。
★ H2SO3是二元中强酸, ![]() ,
, ![]() ,H2SO3只存在于水溶液中,光谱试验证明SO2在水溶液中的状态基本上是SO2·H2O。
,H2SO3只存在于水溶液中,光谱试验证明SO2在水溶液中的状态基本上是SO2·H2O。
★ H2SO3是较强的还原剂,例如:
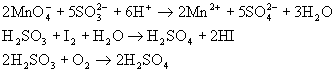
所以空气中长期放置的亚硫酸或亚硫酸盐会被空气中的氧氧化而失去还原性。
★ 氧化性:H2SO3与强还原剂反应时才表现出氧化性。
H2SO3 + H2S → 3S + 3H2O
★ 漂白作用SO2或H2SO3可与某些有机物发生加合作用,而使有机物退色。例如它们能使品红溶液退色。
SO2主要用于生产硫酸和亚硫酸盐,还大量用于生产合成洗涤剂、食品防腐剂、住所和用具消毒剂等。
⒌三氧化硫、硫酸及其盐
⑴三氧化硫
在加热和催化剂存在下可将SO2氧化成SO3。
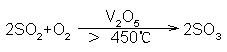
结构:气态SO3为单分子,其分子结构为平面三角形。
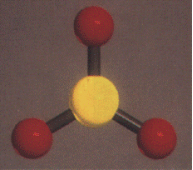
在SO3分子中,硫原子以sp2杂化轨道与3个氧原子形成3个σ键,此外,还以pd2杂化轨道与3个氧原子形成垂直于分子平面的四中心六电子大Π键 ![]() 。即:
。即:

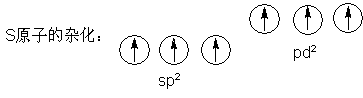
在大Π键中有三个电子原来属于硫原子,而另外三个电子原来分别属于三个氧原子。在固态SO3中,硫原子都采用sp3杂化轨道成键。固体三氧化硫有几种聚合晶型。在不同类型SO3固体中,SO3分子的排列方式不同。γ型晶体为三聚分子,β型晶体为SO3原子团互相连接成的长链,与石棉结构类似,α型晶体也具有类似石棉的结构。
性质:纯三氧化硫是一种无色、易挥发的固体,其熔点为16.8℃,沸点为44.8℃。SO3具有很强的氧化性。例如,当磷和它接触时会燃烧。高温时SO3的氧化性更为显著,它能氧化KI,HBr和Fe,Zn等金属。
三氧化硫极易与水化合生成硫酸,同时放出大量的热:
![]()
因此,SO3在潮湿的空气中呈雾状。
⑵硫酸
结构:在硫酸分子中,硫原子采取sp3杂化轨道与四个氧原子的2个形成2个σ键;另两个则接受硫的电子对分别形成σ配键;与此同时,硫原子的空的3d轨道与两个不在OH基中的氧原子的2p轨道对称性匹配,相互重叠,反过来接受来自2个氧原子的孤对电子,从而形成了附加的(p─d)π反馈配键。
硫酸晶体呈现波纹形层状结构。每个硫氧四面体(SO4原子团)通过氢键与其它4个SO4集团连接。
性质:硫酸是二元强酸,较稳定。浓硫酸具有强吸水性和强氧化性。
★ 强吸水性:浓硫酸的吸水性很强,它除了可作干燥剂外,它还能从纤维和糖中按H:O为2:1的比例夺取H2O,使其碳化。
C12H22O11 → 12C + 11H2O
★ 强氧化性:浓硫酸可以氧化许多金属和某些非金属。
与活泼金属: 3Zn + 4H2SO4(浓) → 3ZnSO4 + S + H2O
4Zn + 5H2SO4(浓) →4ZnSO4 + H2S + H2O
与不活泼金属: Cu + 2H2SO4(浓) → CnSO4 + SO2 + 2H2O
与非金属: C+ 2H2SO4(浓) → CO2 + 2SO2 + 2H2O
2P+ 5H2SO4(浓) → P2O2 + 5SO2 + 5H2O
S+ 2H2SO4(浓) → 3SO2 + 2H2O
冷的浓硫酸(70%以上)能使铁的表面钝化,生成一层致密的保护膜,阻止硫酸与铁的表面继续作用。因此可以用钢罐贮装和运输浓硫酸(80%~90%)。
⑶硫酸盐
硫酸能形成正盐和酸式盐。 ![]() 的结构为四面体。大多数硫酸盐易溶于水,但PbSO4、CaSO4、SrSO4溶解度很小。BaSO4几乎不溶于水且不溶于酸,利用BaSO4的这一特性,可以用BaCl2等可溶性钡盐鉴定
的结构为四面体。大多数硫酸盐易溶于水,但PbSO4、CaSO4、SrSO4溶解度很小。BaSO4几乎不溶于水且不溶于酸,利用BaSO4的这一特性,可以用BaCl2等可溶性钡盐鉴定 ![]() 的存 在。
的存 在。
⒍硫酸的其它含氧酸及其盐
⑴焦硫酸及其盐
冷却发烟硫酸可以析出焦硫酸H2S2O7,无色晶体,焦硫酸的结构式为:
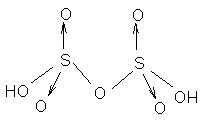
焦硫酸的酸性、吸水性、腐蚀性比硫酸更强。焦硫酸是一种强氧化剂,又是一种良好的磺化剂,工业上用于制造染料、炸药、和其它有机磺酸化合物。
焦硫酸盐可与某些既不溶与水又不溶于酸的金属氧化物(如Al2O3、Fe3O4、TiO2等)共熔,生成可溶与水的硫酸盐。
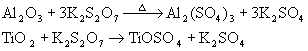
这是分析化学中处理某些固体试样的一种重要方法。
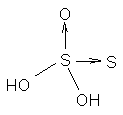
⑵硫代硫酸及其盐
硫代硫酸H2S2O3可看作是硫酸分子中的一个氧原子被硫原子所取代的产物。硫代硫酸极不稳定,至今尚未制得纯品。
亚硫酸亚与硫作用生成硫代硫酸盐。例如,将硫粉与亚硫酸钠一块煮沸,可制得硫代硫酸钠:
![]()
另外,在Na2S和Na2CO3混合溶液(物质的量比为2:1)中通入SO2也可以制得Na2S2O3:
2Na2S + Na2CO3 + 4SO2 → 3Na2S2O3 + CO2
Na2S2O3·5H2O是重要的硫代硫酸盐,俗称海波或大苏打,是无色透明的晶体,易溶于水,其水溶液呈弱碱性。
硫代硫酸盐的重要性质如下:
★ 遇酸分解:
![]()
★ 还原性:
![]()
在纺织工业上用Na2S2O3作脱氯剂。
![]()
在分析化学上用于碘量法滴定。其中产物 ![]() 叫做连四硫酸根离子,其结构式如下:
叫做连四硫酸根离子,其结构式如下:
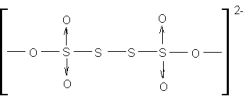
★ 配位作用:
![]()
硫代硫酸钠大量用作照相的定影剂。照相底片上未感光的溴化银在定影液中形成〔Ag(S2O3)2〕3-而溶解。
⑶过硫酸及其盐
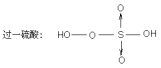
过硫酸可以看作是过氧化氢的衍生物。过氧化氢结构式为H─O─O─H,磺酸基─SO3H结构式为: 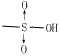 ,H2O2分子中的两个氢原子被─SO3H分步取代,分别得到的产物为过一硫酸H2SO5和过二硫酸H2S2O8。
,H2O2分子中的两个氢原子被─SO3H分步取代,分别得到的产物为过一硫酸H2SO5和过二硫酸H2S2O8。
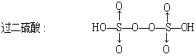
过硫酸具有强氧化性(来自过氧键─O─O─)。它们作为氧化剂参与反应的过程中,过氧键断裂,这两个氧原子的氧化值由原来的-1变为-2,而硫的氧化值保持+6不变。
重要的过二硫酸盐有K2S2O8和(NH4)2S2O8,它们也是强氧化剂。
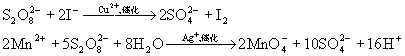
过硫酸盐热稳定性差,例如:
![]()
⑷连二亚硫酸及其盐
连二亚硫酸H2S2O4是二元酸,很不稳定,遇水会立即分解为硫和亚硫酸。
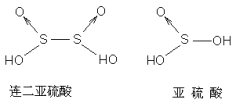
2H2S2O4 + H2O → H2S2O3 + 2H2SO3
2H2S2O3 → S + H2SO3
连二亚硫酸钠Na2S2O3·2H2O俗称保险粉,其稳定性比相应的酸强。
![]()
连二亚硫酸钠是强还原剂。Na2S2O4能将I2、Cu2+、Ag+等还原,能把硝基化合物还原为氨基化合物。空气中的氧能将Na2S2O3氧化。
2Na2S2O4 + O2 + 2H2O→ 2NaHSO3 + 2NaHSO4
连二亚硫酸钠是染料工业和印染工业上常用的还原剂,还广泛用于造纸、食品工业及医学上。
⒎氯磺酸和二氯化硫酰
氯磺酸HSO3Cl可以看作为硫酸分子中的一个羟基被氯原子取代的产物。其结构式为:
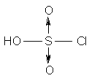
干燥的氯化氢气体与发烟硫酸反应生成氯磺酸:
HCl + SO3 → HSO3Cl
氯磺酸是一种无色、有刺激性气味的气体,遇水发生剧烈水解并爆炸,在潮湿的空气中因水解而发烟。在有机化学上氯磺酸是良好的磺化剂。
二氯化硫酰SO2Cl2相当于硫酸分子中的两个羟基都被氯原子取代的产物,其结构式如下:
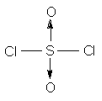
二氧化硫和氯气在催化剂存在条件下能直接化合生成二氯化硫酰:
![]()
二氯化硫酰也是一种无色液体,有强烈的水解作用。二氯化硫酰也用于有机合成工业。
1 / 19