第十二章 氮族、碳族和硼族元素
本章我们主要了解氮族、碳族和硼族元素的通性,熟悉相关分子的结构和稳定性。
§12.1 氮族元素
12.1.1 氮族元素概述
氮族也叫ⅤA族。
氮族元素符号: | N | P | As | Sb | Bi |
价层电子构型: | 2s22p3 | 3s23p3 | 4s24p3 | 5s25p3 | 6s26p3 |
氧化值: | -3~+5 | -3,+3,+5 | -3,+3,+5 | (-3),+3,+5 | +3,(+5) |
最大配位数: | 4 | 6 | 6 | 6 | 6 |
氮族元素的 价层电子构型为ns2np3,电 负性不是很大,所以本族元素形成氧化值为正的化合物的趋势比较明显,化合物只要是共价型的,而且原子愈小,形成共价键趋势也愈大。
氮族元素在自然界的存在形式:
氮: | 主要以单质存在于大气中。 |
磷: | 主要以磷酸盐形式分布在地壳中,如,磷酸钙Ca3(PO4)2,氮磷灰石3Ca3(PO4)2·CaF2。 |
砷、锑、铋: | 主要以硫化物矿存在,如,雄黄4S4As4、辉锑矿Sb2S3、辉铋矿Bi2S3等。 |
12.1.2 氮族元素的单质
氮气是无色、无臭、无味的气体。微溶于水,沸点为-195.8℃。常温下氮气的性质极不活泼,加热时氮气与活泼金属Li、Ca、Mg等反应,生成离子型化合物。
氮分子是双原子分子,两个氮原子以三键结合,电子排布为: ![]() ,由于N≡N键的键能(946kJ/mol)非常大,所以N2是最稳定的双原子分子,氮气表现出高的化学惰性,因此氮气常被用作保护气体。
,由于N≡N键的键能(946kJ/mol)非常大,所以N2是最稳定的双原子分子,氮气表现出高的化学惰性,因此氮气常被用作保护气体。
磷的常见的同素异形体有:白磷、红磷和黑磷。
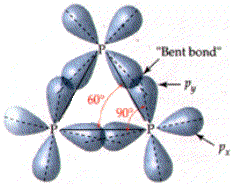
白磷是透明的、柔软的蜡状固体,由P4分子通过分子间力堆积起来,每个磷原子通过其px,py和pz轨道分别和另外3个磷原子形成3个σ键,键角∠PPP为60°,分子内部具有张力,其结构不稳定。所以P4化学性质很活泼,在空气中自燃,能溶于非极性溶剂。
将白磷隔绝空气加热到400℃时可得到红磷。红磷的结构较复杂。一种观点认为:P4分子中的一个P—P键断裂后相互连接起来形成长链结构,所以红磷较稳定,400℃以上才燃烧。红磷不溶于有机溶剂。
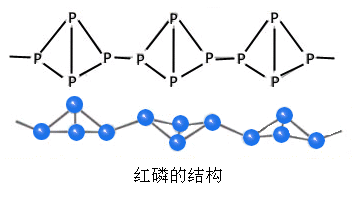
黑磷具有与石墨类似的层状结构,当与石墨不同的是,黑磷每一层内的磷原子并不都在同一平面上,而是相互连接成网状结构。所以黑磷具有导电性,也不溶于有机溶剂。
12.1.3 氮的化合物
⒈ 氮的氢化物
在氮的氢化物中重点学习氨和铵盐。
⑴氨
结构:氨原子以三个不等性杂化轨道与氢原子成键,形成三角锥型结构。
制备:
工业制备法:
![]()
实验室制备法:
![]()
性质:氨是无色气体,有特殊刺激性气味,溶于水呈碱性。氨的化学性质活泼,能与许多物质发生反应。
氧化还原反应:
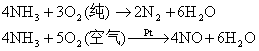
主要体现了氨的强还原性。
加合反应: Ag++ 2NH3 → [Ag(NH3)2]+
取代反应: ![]()
⑵铵盐
铵盐一般为无色晶体,绝大多数易溶于水,在水中都有一定程度的水解,水解反应为:
![]()
![]() 的结构:
的结构: ![]() 中的氮原子采用四个sp3杂化轨道与四个氢原子成键,形成正四面体的空间构型。
中的氮原子采用四个sp3杂化轨道与四个氢原子成键,形成正四面体的空间构型。
![]() 的鉴定:石蕊试纸法和Nessler试剂法。在试液中加碱,加热试液使氨气逸出,用石蕊试纸检验,试纸由红变蓝,用Nessler试纸检验,试纸由白到红棕再到深褐色。反应可表示如下:
的鉴定:石蕊试纸法和Nessler试剂法。在试液中加碱,加热试液使氨气逸出,用石蕊试纸检验,试纸由红变蓝,用Nessler试纸检验,试纸由白到红棕再到深褐色。反应可表示如下:
![]()
固体铵盐的热稳定性差:铵盐的热分解情况因组成铵盐的酸的性质不同而异。
![]()
![]()
非挥发性非氧化性酸的铵盐,分解时只有氨挥发掉,而酸或酸式盐则留在容器中。
![]()
![]()
氧化性酸的铵盐,分解出的氨气被氧化成N2和N2O。
![]()
![]()
⒉ 氮的氧化物
氮的氧化物分子中因所含的N-O键较弱 ,其热稳定性都比较差,它们受热易分解或易被氧化。其中最重要的是NO或NO2。
⑴一氧化氮(NO)
结构:NO的分子轨道电子排布为:(1σ)2(2σ)2(3σ)2(4σ)2(1π)4(2π)1可见分子中有未成对的单电子存在,NO具有顺磁性。NO参与反应时容易失去2π轨道上的一个单电子形成亚硝酰离子NO+。
制备:NO是硝酸生产的中间产物。
工业制法: ![]()
实验室制法: 3Cu + 8HNO3(稀) → 3Cu(NO3)2 + 2NO + 4H2O
性质:NO是无色气体,水中溶解度较小。
2NO + O2 → 2NO2
2NO + Cl2 → 2NOCl(氯化亚硝酰)
Fe2+ + NO → [Fe(NO)]2+(亚硝酰合铁(Ⅰ))
⑵二氧化氮和四氧化氮
结构:NO2中的N以两个sp2杂化轨道与氧原子成键,形成V字型的空间构型,此外分子中还形成一个三中心三电子大∏( ![]() )键。
)键。
![]()
性质:NO2是有特殊臭味的红棕色有毒气体。
NO2冷却时转化为无色的N2O4(g)。
![]()
NO2被水吸收生成硝酸和NO,被NaOH吸收生成硝酸盐和亚硝酸盐。
3NO2 + H2O → 2HNO3 + NO
2NO2 +2NaOH → NaNO3 + NaNO2 + H2O
⒊ 氮的含氧酸及其盐
⑴亚硝酸及其盐
亚硝酸的结构:HNO2中N以两个sp2杂化轨道分别与羟基
氧和氧原子形成σ键,N和O原子之间还形成一个π键,结构如图所示。
亚硝酸的制备:必须在冷溶液中制备。
![]()
![]()
亚硝酸的性质:亚硝酸是一种弱酸, ![]() 。亚硝酸极不稳定,只能存在于很稀的冷溶液中,溶液浓缩或加热时都会分解。
。亚硝酸极不稳定,只能存在于很稀的冷溶液中,溶液浓缩或加热时都会分解。
![]()
亚硝酸根的结构: ![]() 中的N采取两个sp2杂化轨道分别与氧原子形成σ键,此外还形成一个三中心四电子大∏键(
中的N采取两个sp2杂化轨道分别与氧原子形成σ键,此外还形成一个三中心四电子大∏键( ![]() ),离子是V字型结构。
),离子是V字型结构。
亚硝酸盐的制备:用碱吸收等物质的量的NO和NO2。
NO + NO2 + 2NaOH → 2NaNO2 + H2O
亚硝酸盐的性质:除AgNO2是浅黄色不溶性固体外,大多数亚硝酸盐是无色的,一般易溶于水,极毒,是致癌物质。
亚硝酸盐在酸性介质中既有氧化性又有还原性,实际应用中常作氧化剂,其还原产物一般为NO。
![]()
当亚硝酸盐与强氧化剂作用时,才表现出其还原性。
![]()
形成亚硝酸盐的阳离子金属性越强,亚硝酸盐的稳定性越高。例如:AgNO2<NaNO2。
⑵硝酸及其盐
硝酸的结构:HNO3中的N原子采取sp2杂化轨道分别与一个羟基氧和两个氧原子形成3个σ键,N原子中未参与杂化的p轨道中的两个电子与两个非羟基氧在O-N-O间形成三中心四电子∏键( ![]() ),如图所示。
),如图所示。
硝酸的性质:浓硝酸很不稳定,见光受热易分解。
4HNO3 → 4NO2 + O2 +2H2O
硝酸由于挥发而产生白烟,故称为发烟硝酸;硝酸中常因溶有分解出来的NO2而带有黄色或红棕色。
硝酸最典型的性质是它的强氧化性。硝酸可以把碳、磷、硫、碘等许多非金属氧化为高价酸,而其自身被还原为NO。
3C + 4HNO3 → 3CO2 + 4NO + 2H2O
3P + 5HNO3 + 2H2 → 3H3PO4 + 5NO
S + 2HNO3 → H2SO4 + 2NO
3I2 + 10HNO3 → 6HIO3 + 10NO + 2H2O
大部分金属可溶于硝酸,硝酸被还原的程度与金属的活泼性和硝酸的浓度有关。
Cu + 4HNO3(浓) → Cu(NO3)2 + 2NO2 + 2H2O
3Cu + 8HNO3(稀) → 3Cu(NO3)2 + 2NO + 4H2O
4Zn + 10NO3(稀) → 4Zn(NO3)2 + N2O + 5H2O
4Zn + 10NO3(很稀) → 4Zn(NO3)2 + NH4NO3 + 3H2O
可见,金属越活泼,硝酸的浓度越低,HNO3被还原后氮的氧化值越低。
金、铂等不活泼金属能溶于王水(硝酸与浓盐酸以体积比1:3的比例而配制的混合物)中。
Au + HNO3 + 4HCl → H[AuCl4] + NO + 2H2O
3Pt + 4HNO3 + 18HCl → 3H2[PtCl6] + 4NO +8H2
注意:冷的浓硝酸可以使Fe、Al、Cr钝化(浓硝酸将金属表面氧化成一层薄而致密的氧化物保护膜,致使金属不能再与硝酸继续作用)。
浓硝酸还能与有机化合物发生硝化反应。
![]()
硝酸根的结构: ![]() 中的N采取sp2杂化轨道分别与3个O原子形成σ键,N中的为参与杂化的p轨道中的两个电子与3个O的3个p电子形成四中心六电子大∏键(
中的N采取sp2杂化轨道分别与3个O原子形成σ键,N中的为参与杂化的p轨道中的两个电子与3个O的3个p电子形成四中心六电子大∏键( ![]() )。
)。
硝酸盐的性质:几乎所有的硝酸盐都溶于水。硝酸盐固体或水溶液在常温下都比较稳定,水溶液在酸性条件下才有氧化性,固体在高温时才有氧化性,故硝酸盐可用作炸药、火药、焰火中的氧化剂。
硝酸盐受热时分解,分解产物因金属离子性质不同而分为三类:(以金属活动顺序中的排序为准)
K~Mg: ![]()
Mg~Cu: ![]()
Cu以后: ![]()
思考:比较硝酸亚硝酸的酸性、氧化性;比较硝酸盐、亚硝酸盐的热稳定性。
12.1.4 磷的化合物
⒈ 磷的化合物(膦PH3)
结构:三角锥形,类似于NH3。
制备:单质磷在碱溶液中歧化。
P4 + 3KOH + 3H2O → PH3 + 3KH2PO2(次磷酸钾)
此外还可用类似制备氨的方法制备PH3。
复分解法:PH4I + KOH → PH3 + H2O + KI
水解法: Mg3P2 + 6H2O → 2PH3 + 3Mg(OH)2
性质:膦是无色气体,有似大葱臭味,剧毒。有强还原性。
PH3 + 2O2 → H3PO4
⒉磷的氧化物
磷的常见氧化物有五氧化二磷和三氧化二磷。
⑴三氧化二磷
磷在氧气不足的条件下燃烧生成P4O6,简称为三氧化二磷。三氧化二磷的结构如图所示。相当于6个氧原子“插”在P4的四面体的六个棱上。所以P4O6是白色易挥发的蜡状固体,易溶于有机溶剂。
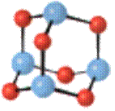
P4O6是亚磷酸酐,与冷水反应较慢,生成亚磷酸。
P4O6 + 6H2O(冷) → 4H3PO3
P4O6在热水中歧化为磷酸和膦(或单质磷)。
P4O6 + 6H2O(热) → 3H3PO4 + PH3
5P4O6 + 182O(热) → 12H3PO4 + 8P
P4O6于氧气进一步反应生成P4O10。
P4O6 + 2O2 → P4O10
⑵五氧化二磷
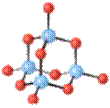
磷在充足的空气中燃烧生成P4O10,简称为五氧化二磷。五氧化二磷的结构如图所示。相当于在P4O6的基本结构单元的各个磷原子的顶上再加上一个氧原子,P4O10是雪花状晶体,且有很强的吸水性,常用作干燥剂。
P4O10 + 6H2O → 4H3PO4
P4O10 + 6H2SO4 → 6SO3 + 4H3PO4
P4O10 + 12HNO3 → 6N2O5 + 4H3PO4
可见P4O10可使硫酸、硝酸等脱水生成氧化物。
⒊ 磷的含氧酸及其盐
磷能形成多种含氧酸。磷的含氧酸按氧化值不同可分为次磷酸H3PO2、亚磷酸H3PO3和磷酸H3PO4等。
⑴次磷酸及其盐
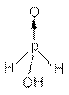
性质:次磷酸是一元中强酸, ![]() 。H3PO2是强还原剂,能在溶液中将AgNO3、HgCl2、CuCl2等重金属盐还原为金属单质。 次磷酸盐多易溶于水,也是强还原剂。
。H3PO2是强还原剂,能在溶液中将AgNO3、HgCl2、CuCl2等重金属盐还原为金属单质。 次磷酸盐多易溶于水,也是强还原剂。
结构:
⑵亚磷酸及其盐
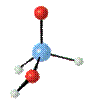
性质:H3PO3是二元中强酸, ![]() ,
, ![]() 。
。
H3PO3是强还原剂,受热易歧化。
H3PO3 + 2Ag+ + H2O → H3PO4 + 2Ag + 2H+
![]()
结构:
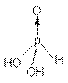
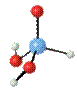
亚磷酸能形成正盐和酸式盐。碱金属和钙的亚磷酸盐易溶于水,其他金属的亚磷酸盐都难溶。亚磷酸盐也是较强的还原剂。
⑶磷酸
性质:H3PO4是三元中强酸, ![]() ,
, ![]() ,
, ![]() 。
。
正磷酸可形成三种类型的盐:正盐、磷酸一氢盐、磷酸二氢盐。一般正磷酸盐比较稳定,不易分解。
结构:
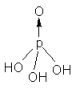
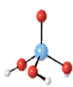
磷酸的三种盐类溶解性和水解性比较如下:
| M3PO4 | M2HPO4 | MH2PO4 |
溶解性: | 大多数难溶于水(除K+,Na+,铵离子外) | 大多数易溶于水 | |
水溶液酸碱性: | PH>7 | PH>7 | PH<7 |
原因: | 水解为主 | 水解>解离 | 水解<解离 |
磷酸盐中最重要的的是钙盐。工业上利用天然磷酸钙生产磷肥,反应如下:
Ca3(PO4)2 + 2H2SO4 + 4H2O → Ca(H2PO4)2 + 2(CaSO4·2H2O)(过磷酸钙(磷肥))
![]() 的鉴定:将磷酸盐与过量的钼酸铵(NH4)2MoO4及适量的浓硝酸混合后加热,可慢慢生成黄色的磷钼酸铵沉淀,反应为:
的鉴定:将磷酸盐与过量的钼酸铵(NH4)2MoO4及适量的浓硝酸混合后加热,可慢慢生成黄色的磷钼酸铵沉淀,反应为:
![]()
磷酸受热后脱水可形成焦磷酸、聚磷酸、偏磷酸等。
焦磷酸及其盐
两个磷酸分子脱去一个水分子及得焦磷酸H4P2O4。焦磷酸是无色玻璃状物质,易溶于水。在冷水中缓慢转化为磷酸。
H4P2O4 + H2O → 2H3PO4
焦磷酸为四元中强酸 ,结构为: 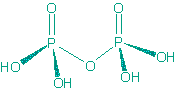
常见的焦磷酸盐为M2H2P2O7和M4P2O7两类。 ![]() 具有配位能力,例如:
具有配位能力,例如:
![]()
![]()
所以焦磷酸盐可用于硬水软化和无氰电镀。
偏磷酸及其盐
偏磷酸指一个H3PO4脱去一个H2O即HPO3。若为n个H3PO4脱去n个H2O,即为多聚偏磷酸,常见的有三聚偏磷酸和四聚偏磷酸。脱水过程以四聚偏磷酸(HPO3)4为例,图示如下:
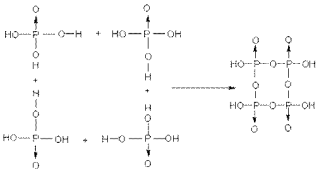
聚磷酸是指n个H3PO4脱去n-1个水,如焦磷酸即为二聚磷酸;三聚磷酸的形成可图示如下:
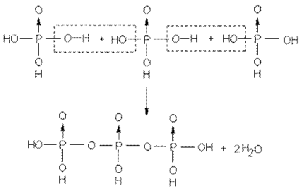
聚磷酸盐同样具有配位能力。
![]()
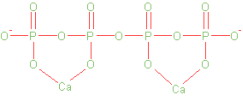
小结:
★ 缩合度增加,酸性增强。
| H5P3O10 | H4P2O7 | H3PO4 |
|
| 2.9×10-2 | 6.7×10-3 |
| 10-2 | 5.3×10-3 | 6.2×10-8 |
| 10-3 | 2.2×10-7 | 4.5×10-13 |
★ 鉴别正磷酸、焦磷酸和偏磷酸的方法:
| 正磷酸 | 焦磷酸 | 偏磷酸 |
AgNO3 | 黄色↓ | 白色↓ | 白色↓ |
蛋白质 |
|
| 白色↓ |
⒋磷的卤化物
磷可以形成三卤化磷PX3和五卤化磷PX5。
最重要的卤化物为三氯化磷和五氯化磷。在室温下,三氯化磷是无色液体,五氯化磷是白色晶体,该晶体是无色晶体,晶体中含有[PCl4]+和[PCl6]-离子。
磷的卤化物最重要的性质就是水解性。
PCl3 + 3H2O → H3PO3 +3HCl
PCl5 + 4H2O → H3PO4 +5HCl
| PCl3 | PCl5 |
结构 | 三角锥 | 三角双锥 |
|
|
|
中心原子杂化类型 | 不等性sp3 | sp3d |
12.1.5 砷、锑、铋的化合物
⒈砷、锑、铋的氢化物
砷、锑、铋的氢化物分别是:胂AsH3、 ![]() SbH3、
SbH3、 ![]() BiH3。这些氢化物都是无色液体,结构与氨类似,均为三角锥形。性质变化规律如下:
BiH3。这些氢化物都是无色液体,结构与氨类似,均为三角锥形。性质变化规律如下:
★ 熔、沸点从胂到 ![]() 由低到高。
由低到高。
★ 稳定性从胂到 ![]() 由高到低。
由高到低。
★ 碱性从胂到 ![]() 由强到弱。
由强到弱。
胂、 ![]() 、
、 ![]() 均极毒。胂有似大蒜的刺激性气味,室温下在空气中燃烧:
均极毒。胂有似大蒜的刺激性气味,室温下在空气中燃烧:
2AsH3 + 3O2 → As2O3 +3H2
在缺氧条件下,胂受热分解:
![]()
检验生物体是否含砷中毒,利用的是AsH3的热不稳定性和还原性。
⒉ 砷、锑、铋的氧化物
砷、锑、铋可形成两类氧化物,即M2O3和M2O5,M2O3是相应的亚酸的酸酐,M2O5是相应的正酸的酸酐。
砷、锑、铋的单质在空气中燃烧和焙烧它们的硫化物可制得它们的M2O3。
| As2O3 | Sb2O3 | Bi2O3 |
颜色、状态 | 白色粉末 | 白色固体 | 黄色粉末 |
水溶性 | 微溶 | 难溶 | 极难溶 |
酸碱性 | 两性偏酸 | 两性 | 碱性 |
晶体结构 | 分子晶体 | 分子晶体 | 离子晶体 |
常温为双聚分子 | As4O6 | Sb4O6 |
|
三氧化二砷As2O3,俗称砒霜,剧毒。主要用于制造杀虫剂、除草剂以及含砷药物。
As2O5为白色;Sb2O5为淡黄色;Bi2O5为红棕色,极不稳定。
⒊砷、锑、铋的氢氧化物及其含氧酸
酸碱性递变:

M(Ⅲ)的还原性:
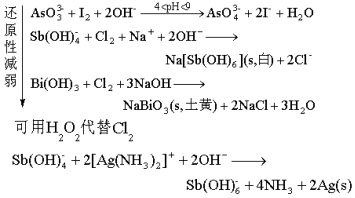
M(Ⅴ)的氧化性:
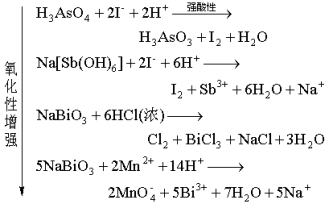
注意下面反应发生的条件,并解释为什么?
![]()
![]()
⒋砷、锑、铋的盐
砷、锑、铋难以形成M5+,但在强酸溶液中可以形成M3+。砷、锑、铋的盐在水中都易水解。AsCl3的水解类似于PCl3,产物为两种酸。
AsCl3 + 3H2O → H3AsO3 + 3HCl
锑、铋的盐水解为碱式盐。
Sb2(SO4)3 + 2H2O→ (SbO)2SO4(s) + 2H2SO4
BiCl3 + H2O → BiOCl(s) + 2HCl
Sb3+、Bi3+具有一定的氧化性。
2Sb3+ + 2Sn → 2Sb + 3Sn2+
这是鉴定Sb3+的特征反应。
2Bi3+ + 3[Sn(OH)4]2- + 6OH- → 2Bi + 3[Sn(OH)6]2-
这是鉴定Bi3+的特征反应。
⒌砷、锑、铋的硫化物
硫化物:
As2S3(黄) | Sb2S3(橙) | Bi2S3(黑) |
As2S5(黄) | Sb2S5(橙) | Bi2S5(不能形成) |
硫化物的性质:
⑴不溶于水和稀酸。
⑵配位溶解(浓HCl)。
![]()
![]()
![]()
As2S3、As2S5不溶。
⑶碱溶
NaOH
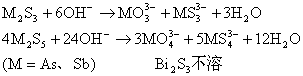
Na2S
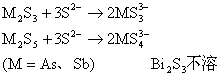
⑷氧化碱溶
![]()
⑸与氧化性酸(HNO3)作用
![]()
§12.2 碳族元素
12.2.1 碳族元素概述
碳族元素符号: | C | Si | Ge | Sn | Pb |
价层电子构型: | 2s22p2 | 3s23p2 | 4s24p2 | 5s25p2 | 6s26p2 |
氧化值 | -4,+2,+4 | +4 | (+2),+4 | +2,+4 | +2,(+4) |
最大配位数: | 4 | 4 | 4 | 6 | 6 |
碳族元素的价层电子构型为2s22p2,得失电子都较难,这决定了碳族元素成键的主要倾向是共价键。
碳族元素在自然界的存在形式:
碳:金刚石、石墨;煤、石油、天然气;碳酸盐;CO2
硅:SiO2和硅酸盐。
锗:主要以硫化物形式存在:4Ag2S·GeS2(硫银锗矿)和2PbS·GeS2(硫铅锗矿),请注意铅和锗的氧化值,
体会到惰性电子对效应的存在。
锡:锡石(SnO2)
铅:方铅矿(PbS),白铅矿(PbCO3)
12.2.2 碳族元素的单质
单质碳存在着同素异形体:
无定型碳: 木炭、焦炭、骨碳。
金刚石: 原子晶体,硬度大,熔点高。
石墨: 层状晶体。
足球烯(富勒烯): C60,C70等。
单质硅也存在着同素异型体:无定型体和晶体硅,后者是原子晶体。
单质锗:是灰白色金属,结构类似于金刚石。
单质锡:三种同素异型体:
![]()
低温下,白锡变成粉末,称之为"锡疫"。
铅:质软,能阻挡X射线,可以用作核反应堆的保护屏。
12.2.3 碳的化合物
1. 碳的氧化物
⑴一氧化碳(CO)
结构:CO与N2为等电子体(14e-),结构相似,均有三键。
![]()
![]()
性质:
① 作为配位体形成羰基配合物,Fe(CO)5,Ni(CO)4,Co2(CO)8,其中C是配位原子。
② CO作为还原剂,在冶金工业中得到广泛应用。
3CO(g) + Fe2O → 2Fe(s) + 3CO2(g)
CO(g) + CuO(s) → Cu(s) + CO2(g)
CO(g) + PdCl2(aq) + H2O → Pd(s) + CO2 + 2HCl(aq)
此反应因生成黑色Pb,可用于检验CO的存在。
③ CO有毒,空气中CO的体积比达到1∕800,人在半小时那就会死亡。因为CO与血液中的血红蛋白结合,使之失去载氧能力,人缺氧而窒息死亡。
⑵二氧化碳(CO2)
经典的分子结构:O=C=O,后来人们测得CO2中C与O间的键长为116pm,介于双键键长与三键键长之间( ![]() 中的C=O键长为124pm,CO三键键长为113pm),为此人们提出CO2中应存在以下键型:C与O间除了有σ键外,在CO2
中的C=O键长为124pm,CO三键键长为113pm),为此人们提出CO2中应存在以下键型:C与O间除了有σ键外,在CO2
分子中尚存在2个三中心四电子大∏键( ![]() )
) ![]()
2. 碳酸及其盐
CO2溶于水,大部分以CO2·�������H2O形式存在,极小部分是以H2CO3的形式存在,也就是说CO2溶于水后,水溶液中存在以下平衡:
![]()
![]()
![]()
应指出的是,上述解离常数是把CO2看作全部形成碳酸,这与事实不符,考虑溶液中的平衡,H2CO3的实际解离常数为: ![]() 。
。
★ 碳酸盐的热稳定性:
① 正盐>酸式盐>酸,即M2CO3>MHCO3>H2CO3。例如Na2CO3很难分解,NaHCO3在270℃分解,H2CO3在室温下即可分解。
![]()
![]()
H2CO3 → H2O + CO2
② 同一族的金属的碳酸盐的稳定性从上到下增加。
例如:
碳酸盐 | BeCO3 | MgCO3 | CaCO3 | SrCO3 | BaCO3 |
分解温度/℃ | 100 | 540 | 900 | 1290 | 1360 |
r(M2+)增大,稳定性增加,分解温度增高。
③ 过渡金属碳酸盐稳定性差
碳酸盐 | CaCO3 | PbCO3 | ZnCO3 | FeCO3 |
分解温度/℃ | 900 | 315 | 350 | 282 |
M2+价层电子构型 | 8e- | (8+2)e- | 18e- | (9-17)e- |
上述热稳定性规律可用离子极化理论解释:
在 ![]() 内部:C(4+)对O2-有极化能力,而在M2+与
内部:C(4+)对O2-有极化能力,而在M2+与 ![]() 之间:
之间: 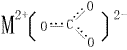
M2+对邻近的O2-有反极化作用,抵消C(4+)对O2-的极化作用,消弱了C···O键,反极化作用的大小与M2+的半径,价层电子构型有关,M2+的半径越小(如Be2+),极化力越强,MO结合越密切,C-O键断开,分解温度就越低;非8e-构型M2+极化力大,所以,分解温度也低。
★ 碳酸盐的溶解性:
对难溶盐来说,酸式盐溶解度大于正盐,例如:Ca(HCO3)2易溶于水,而CaCO3难溶于水。地表层中的碳酸盐矿石在CO2和水的长期侵蚀下能部分的转变为Ca(HCO3)2而溶解。
CaCO3+ CO2 + H2O → Ca(HCO3)2
石灰岩地域出现钟乳石景观与此有关。
对易溶盐来说,规律恰好相反,酸式盐溶解度小于正盐。
碳酸盐 | Na2CO3 | NaHCO3 | K2CO3 | KHCO3 |
S (100℃)g/100g H2O | 45 | 16 | 156 | 60 |
这是由于氢键存在, ![]() 之间形成二聚物或多聚物 缘故。
之间形成二聚物或多聚物 缘故。
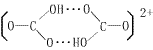
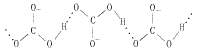
★ 碳酸盐的水解性:
![]()
![]()
溶液中含有 ![]() 、OH-等,此时,加入金属离子生成的沉淀类型是什么?
、OH-等,此时,加入金属离子生成的沉淀类型是什么?
金属离子加入碳酸盐后,生成沉淀的类型:
① 氢氧化物碱性强的的金属离子与之反应生成碳酸盐沉淀。例如:Ba2+,Sr2+,Ca2+和Ag+等。
![]()
② 氢氧化物碱性较弱的金属离子与之反应生成碳酸羟盐(碱式碳酸盐)沉淀。例如,Pb2+,Bi3+,Cu2+,Cd2+,Zn2+,Hg2+,Co2+,Ni2+和Mg2+等。
![]()
![]()
③ 水解性强,两性的金属离子与之反应生成氢氧化物沉淀。例如:Al3+,Fe3+,Cr3+,Sn2+,Sn4+,Sb3+等。
![]()
![]()
 12.2.4 硅的化合物
12.2.4 硅的化合物
1.硅的氧化物:SiO2(硅石)
无定型体:石英玻璃、硅藻土、燧石。
晶体:天然SiO2晶体称为石英,纯净的石英称为水晶,属于原子晶体,用于制作光学仪器及工艺品等。
含杂质的石英:玛瑙、紫晶。
SiO2的性质:SiO2属于酸性氧化物,试想它与碱反应的产物。另外,SiO2与HF反应的实用性:
SiO2 + 2NaOH → Na2SiO3 + H2O
SiO2 + Na2CO3 → Na2SiO3 + CO2
SiO2 + 4HF → SiF4 + 2H2O
2.硅酸及其盐
硅酸:H2SiO3(原硅酸H4SiO4的脱水形式)二元弱酸: ![]() ,可见硅酸酸性比碳酸弱,由此可想到制备硅酸可用酸性比硅酸强的二氧化碳、氯化铵、氯化氢等与硅酸钠反应:
,可见硅酸酸性比碳酸弱,由此可想到制备硅酸可用酸性比硅酸强的二氧化碳、氯化铵、氯化氢等与硅酸钠反应:
Na2SiO3 + 2NH4Cl → H2SiO3 + 2NaCl + 2NH3
Na2SiO3 + 2HCl → H2SiO3 + 2NaCl
产物H2SiO3,开始为单分子硅酸溶于水,后聚合成多硅酸,形成硅酸溶胶,当浓度大时或加入电解质时,形成凝胶,经过干燥后得到白色透明固体。它具有许多极细小的孔隙,表面积大,吸附能力强,常用作干燥剂和吸附剂载体。浸透过CoCl2的硅胶称为变色硅胶,干燥时呈蓝色,吸水饱和后呈粉红色。
硅酸盐:除了Na2SiO3(俗称水玻璃)为可溶性硅酸盐外,大多数硅酸盐难溶于水,且有特征颜色。 水中花园(难溶于水的硅酸盐)
硅酸盐结构复杂,以SiO4四面体为结构单元,可连接成线层、主体网状。 一般以氧化物形式表示硅酸盐,
例如:白云石 K2O·3Al2O3·6SiO2·2H2O
泡沸石 Na2O·Al2O3·2SiO2·nH2O
铝硅酸盐 人工合成的铝硅酸盐称为分子筛,天然泡沸石 与人工合成分子筛都具有多孔多穴结构,直径比孔穴小的分子能进入孔穴中,直径比孔道大的分子被拒之于外,起着筛选分子的作用。人们可根据不同需要制备不同结构、不同孔径的分子筛。广泛用于石油化工、冶金医疗等工业。
3.硅的卤化物
卤化物 | SiF4 | SiCl4 | SiBr4 | SiI4 |
聚集状态 | g | l | l | s |
其沸点依次升高,试用学过的知识解释该规律。
水解性: SiCl4 + 3H2O → H2SiO3 + 4HCl
SiF4 + 3H2O → H2SiO4 + 4HF
SiF4 + 2HF → H2[SiF6]
12.2.5 锡、铅的化合物
1.氧化物的酸碱性
均为两性,当酸碱强度不等。
M(Ⅱ): ![]()
![]()
![]() (加HNO3或HAc不能加HCl、H2SO4)
(加HNO3或HAc不能加HCl、H2SO4)
![]()
M(Ⅳ):
α-锡酸能溶于酸也能溶于碱,β-锡酸不溶于酸也不溶于碱。
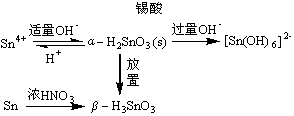
Sn + 4HNO3(浓) → H2SnO3 + 4NO2 + H2O
总之,锡、铅的氢氧化物的酸碱性规律如下:
★ 同一元素高氧化值氢氧化物比低氧化值氢氧化物的酸性强;
★ 同一氧化值的不同元素,遵循同一主族由上到下碱性增强的规律。相对而言,Pb(OH)2碱性最强,Sn(OH)4酸性最强,所以称之为锡酸。

2.锡、铅(Ⅱ、Ⅳ)化合物的氧化还原性
![]()
![]()
Sn(Ⅱ)具有强还原性
酸性:
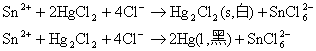
此反应是鉴定Sn2+或Hg2+的反应。
碱性:
![]()
此反应是鉴定Bi3+的反应。
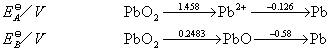
Pb(Ⅳ)具有强氧化性
5PbO2 + 2Mn2+ + 4H+ → 2MnO4- + 5Pb2+ + 2H2O
3PbO2 → Pb3O4 + O2
Pb3O4,俗称铅丹,红色。与亚麻仁油混合后作为油 灰涂在管子的衔接处,防止漏水。Pb3O4可看作是Pb2PbO4(原铅酸的Pb(Ⅱ)盐)
Pb2PbO4+ 4HNO3 → 2Pb(NO3)2 + PbO2 + H2O
3.锡、铅的盐类
⑴水解
锡、铅的氢氧化物是两性的,因此其盐类易水解:
Sn2+ + H2O + 2Cl- → Sn(OH)Cl(s,白) + HCl
Sn4+ + 6H2O → H2[Sn(OH)6]( α-锡酸) + 4H+
![]()
⑵铅(Ⅱ)盐的溶解性
少数可溶: | Pb(NO3)2,Pb(Ac)2(味甜,俗称铅糖弱电解质),可溶性铅盐均有毒。 |
多数难溶: | PbCl2,PbSO4,PbI2(金黄),PbCrO4(黄)。 |
溶解方法: | PbCl2溶于热水和浓HCl(生成 |
| PbSO4溶于浓H2SO4:PbSO4 + H2SO4 → Pb(HSO4)2 |
| PbI2溶于KI:PbI2 + 2KI → K2PbI4 |
| PbCrO4溶于HNO3: |
| 亦溶于 碱: |
4.铅的硫化物
SnS(棕),SnS2(黄),PbS(黑),不存在PbS2。
⑴均不溶于水,不溶于稀HCl。
⑵溶于浓HCl(配位溶解)
![]()
![]()
![]()
⑶碱溶(SnS,PbS碱性强,不溶于碱)
![]()
![]()
⑷氧化碱溶(SnS2,PbS不溶)
![]()
⑸氧化溶解
![]()
§12.3 硼族元素
12.3.1 硼族元素概述
硼族(ⅢA)包括:硼(B),铝(Al), 镓(Ga), 铟(In), 铊(Tl),价电子构型为:ns2np1 ,硼族元素的价电子数(3个电子)<价层轨道数(1个s轨道个+3个p轨道),所以硼族元素是缺电子元素。所以硼族元素易形成缺电子化合物。 例如:BF3
缺电子化合物: 成键电子对数<价层轨道数
缺电子化合物是典型的Lewis酸,
a. 易形成配位化合物,例如:HF+BF3→HBF4
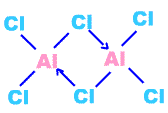 b. 易形成双聚物,例如:Al2Cl6
b. 易形成双聚物,例如:Al2Cl6
12.3.2 硼族元素的单质
单质硼有多种同素异形体,无定形硼为棕色粉末,晶体硼呈灰黑色.单质硼的硬度近似于金刚石,硼的电阻很大,但它的电导率却随着温度的升高而增大。
晶态单质硼有多种变体,它们都以B12正二十面体为基本的结构单元。该二十面体由12个B原子组成,20个接近等边三角形的棱面相交成30条棱边和12个角顶,每个角顶为一个B原子所占据。由于B12二十面体的连接方式不同,键也不同,形成的硼晶体类型也不同。
α一菱形硼是由B12单元组成的层状结构,该晶体属于原子晶体,因此晶态单质硼的硬度大,熔点高,化学性质不活泼;无定形硼则比较活泼。
铝是银白色有光泽的轻金属,具有良好的导电性和延展性;是很重要的金属材料和结构材料,常用以制作导线、和日用器皿。
镓、铟、铊都是软金属,物理性质相近,熔点都较低,镓的熔点比人体体温还低。镓、铟、铊可用于生产新型半导体材料。
12.3.3 硼的化合物
下面列举了一些重要硼的化合物
硼化物 | 颜色和状态 | 密度(g/cm-3) | 熔点(℃) | 受热时的变化 | 溶解度(g/100g H2O) |
四硼酸钠 (硼砂)NaB4O7×10H2O | 坚硬白色晶体 | 1.73 (无水为2.4) |
| 加热后首先熔化,然后膨胀失去结晶水。最后变为玻璃状物质。NaB4O7×H2O在200℃时仍稳定,400℃以上才完全脱水。 | 2.01(20℃)水溶液呈碱性,也能溶于甘油,却不溶于酒精。 |
硼酸 H3BO3 | 六角形晶体,发珠光的白色鳞状物 | 1.46 | 171.0 | 107℃时失去水,变为偏硼酸HBO2,在140℃~160℃时变为焦硼酸H2B4O7(四硼酸),红热时变为B2O3 | 4.74(20℃)23.3(90℃)溶于水后,有正、偏和焦型的离子,也能溶于甘油,酒精及醚中 |
三氧化二硼 B2O3 | 无色透明玻璃状物 | 2.55 | 450.0 |
| 1.1(0℃)15.7(100℃)极易吸水,吸湿后变为混浊状态,也能溶于酒精 |
三氟化硼 BF3 | 无色气体 | 3.077g/L(STP) | -127.1 | -100℃沸腾 | 在水中溶解 |
氮化硼 BN | 白色,像滑石一样的分状物 | 2.18 2.34 | 2967 3300(加压) | 4930℃升华加热时难被氧化。也不与Cl2作用,红热时与H2O作用放出NH3 | 不溶于水,不与酸,强碱溶液作用。 |
1. 硼的氢化物
硼与氢可形成许多共价型氢化物,按组成可分为两大系列,通式分别为:BnHn+6(B4H10),BnHn+4(B2H6,B5H9,B6H10),称为硼烷。最简单的硼烷是乙硼烷(B2H6)。硼氢化合物的分子结构不能仅用一般的共价键来表示。因为硼原子是缺电子原子,硼烷分子内所有价电子的数不能满足一般共价键所需要的数目。在B2H6分子中,共有14个价轨道,而只有12个价电子,所以B2H6是缺电子化合物。
乙硼烷的结构: 在B2H6分子中,有8个价电子用于2个B原子各与2个H原子形成4个B─Hσ键,这4个σ键在同一平面上。剩下的4 个价电子在2个B原子和另外2个H原子之间形成了垂直于上述平面的2个三中心两电子键,一个在平面之上,另一个在平面之下,每一个三中心两电子键是由1个H原子和2个B原子共用2个电子构成的。这个H原子把2个B原子连接起来,具有桥状结构,我们称这个H原子为“桥氢原子”。
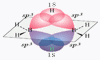
乙硼烷的性质: 常温下,B2H6和B4H10(丁硼烷)为气体,B5~B8为液体,B10H14及其它高硼烷都是固体。硼烷多数有毒,有令人不适的特殊气味,且不稳定。乙硼烷(B2H6)是无色气体,用LiH,NaH或NaBH4与卤化硼作用可以制备B2H6
(1)B2H6是非常活泼的物质,暴露于空气中易燃烧或爆炸,并放出大量的热:
![]()
(2) B2H6易水解释放出氢气,生成硼酸: ![]()
(3)B2H6与LiH反应,能生成一种比B2H6的还原性更强的还原剂硼氢化锂LiBH4 :
![]()
LiBH4为白色盐型氢化物,溶于水或乙醇,无毒,化学性质稳定。广泛用于有机合成,是重要的还原剂。
(4)生成配合物:
![]()
2. 硼的含氧化合物
由于硼与氧形成的B-O键键能大(B-O键键能为:523kJ×mol-1),所以硼的含氧化合物具有很高的稳定性。构成硼的含氧化合物的基本单元是平面三角形的BO3和四面体形的BO4,这是由硼元素的亲氧性和缺电子性质所决定的。
(1)三氧化二硼(B2O3)
B2O3是白色固体,晶态B2O3比较稳定,熔点为460℃。B2O3能被碱金属、镁、铝还原为单质硼:
B2O3+ Mg→2B + 3MgO
B2O3易溶于水,生成硼酸:
B2O3+ 3H2O → 2H3BO3
但在热的水蒸气中则生成挥发性的偏硼酸HBO2:
B2O3+ H2O→ 2HBO2
制备B2O3的一般方法是加热硼酸H3BO3使之脱水:
![]()
(2)硼酸
硼酸包括原硼酸H3BO3、偏硼酸H3BO2和多硼酸xB2O3×yH2O。原硼酸通常又称为硼酸。将纯的硼砂(Na2B4O7·10H2O)溶于沸水中并加入盐酸,放置后可析出硼酸:
Na2B4O7+ H2SO4 + 5H2O→ 4H3BO3+Na2SO4
结构:在H3BO3的晶体中,每个B原子以三个sp2杂化轨道与三个O原子结合成平面三角形结构,每个O原子除以共价键与1个B原子和1个H原子相结合外,还通过氢键与另一个H3BO3单元中的H原子结合而连成片层结构,层与层之间则以微弱的范德华力相吸引。所以硼酸晶体是片状的,有滑腻感,可作润滑剂。
性质:H3BO3是白色片状晶体,微溶于水(0℃时溶解度为6.35g/(100gH2O)),但在热水中溶解度较大(100℃时溶解度为27.6g/(100gH2O))。
H3BO3是一元弱酸,由于B是缺电子原子,它加合了来自H2O分子中的OH而释放出离子:
H3BO3+ H2O ![]() B(OH)4+ H+
B(OH)4+ H+ ![]() =5.8×10-10
=5.8×10-10
表明了硼酸是缺电子化合物,是一个典型的路易士酸。其酸性可因加入甘露醇或甘油(丙三醇)而大为增强:
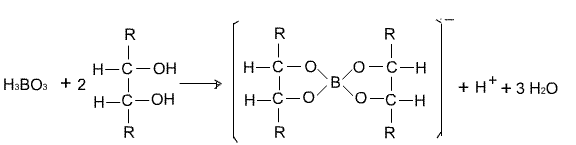
硼酸和甲醇或乙醇在浓H2SO4存在的条件下,生成硼酸酯:
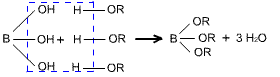
硼酸酯在高温下燃烧挥发,产生特有的绿色火焰,此反应可用于鉴定含硼化合物的存在。
硼酸加热脱水先生成偏硼酸HBO2,继续加热变成B2O3。
2H3BO3 ![]() 2HBO2+2H2O
2HBO2+2H2O ![]() B2O3+ 3H2O
B2O3+ 3H2O
(3)硼酸盐
硼酸盐有偏硼酸盐、原硼酸盐、和多硼酸盐等。最重要的硼酸盐是四硼酸钠,俗称硼砂。硼砂的分子式为Na2B4O5(OH)4·8H2O习惯上也常写作Na2B4O7·10H2O)。
四硼酸根阳离子的立体结构:在四硼酸根中有两个BO3平面三角形和两个BO4四面体通过共用角顶O原子而联结起来。
性质:硼砂是无色半透明的晶体或白色结晶粉末。在空气中容易失水风化,加热到350℃~400℃左右,失去全部结晶水成无水盐,在878℃熔化为玻璃体。熔融状态的硼砂能溶解一些金属氧化物,形成偏硼酸盐,并依金属的不同而显示出特征颜色,例如:
Na2B4O7 + CoO ![]() Co(BO2)2·2NaBO2 (蓝色)
Co(BO2)2·2NaBO2 (蓝色)
Na2B4O7 + NiO ![]() Ni(BO2)2·2NaBO2 (棕色)
Ni(BO2)2·2NaBO2 (棕色)
此反应可用于焊接金属时除锈,也可以鉴定某些金属离子,这在分析化学上称为硼砂珠试验。
硼砂是一个强碱弱酸盐,可溶于水,在水溶液中水解而显示较强的碱性:
[B4O5(OH)4]2- + 5H2O ![]() 4H3BO3+2OH-
4H3BO3+2OH- ![]() 2H3BO3 + 2B(OH)4-
2H3BO3 + 2B(OH)4-
硼砂水解时得到等物质的量的酸(H3BO3)和碱(B(OH)4-),所以此水溶液具有缓冲作用。硼砂易于提纯,水溶液又显碱性,在实验室中常用它配制缓冲溶液或作为标定酸浓度的基准物质。在工业上还可用做肥皂和洗衣粉的填料。
硼砂珠试验可看作是熔融的酸性氧化物B2O3和碱性金属氧化物作用生成有特征颜色的偏硼酸盐玻璃,所以B2O3也有硼砂珠试验,例如:
B2O3 + CuO ![]() Cu(BO2)2 蓝色
Cu(BO2)2 蓝色
B2O3 + NiO ![]() Ni(BO2)2绿色
Ni(BO2)2绿色
在BO3平面三角形结构中,B原子以sp2杂化轨道与O原子结合。(如下右图所示)
在BO4四面体结构中,B原子以sp3杂化轨道与O原子结合。(如下左图所示)
![]()
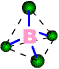
3 硼的卤化物
硼与氢可形成许多共价型氢化物,按组成可分为两大系列,通式分别为:BnHn+6(B4H10),BnHn+4 (B2H6,B5H9,B6H10),称为硼烷。最简单的硼烷是乙硼烷(B2H6)。
硼氢化合物的分子结构不能仅用一般的共价键来表示。因为硼原子是缺电子原子,硼烷分子内所有价电子的数不能满足一般共价键所需要的数目。在B2H6分子中,共有14个价轨道,而只有12个价电子,所以B2H6是缺电子化合物。
卤素都能和硼形成硼的卤化物,即三卤化硼。
制备:通常可用硼与卤素直接反应制得三卤化硼:
2B+3X2 → 2BX3
也可以萤石,浓H2SO4和B2O3反应制备BF3:
B2O3+3CaF2+3 H2SO4→ 2BF3+3CaSO4+3H2O
用B2O3与HF酸作用,可制得BF3:
B2O3+6HF→ 2BF3+3H2O
用置换法,使BF3与AlCl3或AlBr3反应,可得BCl3或BBr3:
BF3(g)+ AlCl3 → AlF3+ BCl3
BF3(g)+ AlBr3 → AlF3+ BBr3
用卤化法,以B2O3和C为原料 ,通入Cl2气,,也可制备BCl3:
B2O3+3C+3Cl2 → 2BCl3+3CO
结构:三卤化硼的分子结构都是平面三角形(如下图),表明B原子都是以sp2杂化轨道与卤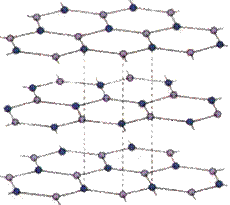 原子形成σ键。
原子形成σ键。
![]()
性质:三卤化硼都是共价化合物,熔﹑沸点均很低,并有规律地按F﹑Cl﹑B﹑I顺序而逐渐增高,它们的挥 发性随相对分子质量的增大而降低。
BF3是无色的有窒息气味的气体,不能燃烧,BF3水解得到氟硼酸H[BF4]:
4BF3+3H2O → 3H[BF4]+H3BO3
体现出BF3是缺电子化合物,是很强的Lewis酸。氟硼酸是强酸,仅以离子状态存在于水溶液中。
BCl3略加压力即可液化,它是无色具有高折射率的液体。在潮湿的空气中发烟并在水中强烈水解:
BCl3+3H2O → H3BO3+3HCl
4. 氮化硼
氮化硼是一种新型的无机合成材料。在873K时, B2O3与NH3反应可制得氮化硼BN。BN与O2是等电子体。等电子体常表现出相似的结构和相似的性质。
BN有三种晶型:
⑴无定型(类似于无定型炭)
⑵六方晶型(类似于石墨)它又称为白石墨,是一种优良的耐高温润滑剂。
⑶立方晶型(类似于金刚石),硬度如金刚石,用作磨料。
12.3.4 铝的化合物
铝是典型的两性元素,铝的单质和化合物既能溶于酸又能溶于碱而呈现典型的两性。
1. 氧化铝和氢氧化铝
氧化铝Al2O3有多种晶型,其中两种主要变体是α-Al2O3和γ-Al2O3。
α-Al2O3称为刚玉,熔点高,硬度大,不溶于酸、碱。
γ-Al2O3称为活性氧化铝,可溶于酸、碱,可用作催化剂载体。
有些氧化铝载体基本上是透明的,因含有少量杂质而呈现鲜明的颜色。红宝石含有极微量铬的氧化物,蓝宝石含有铁和钛的氧化物,黄晶含有铁的氧化物。
红宝石(Cr3+) 蓝宝石(Fe3+,Cr3+) 黄玉/黄晶(Fe3+)
氢氧化铝是两性氧化物,它溶于酸生成 ![]() 。
。
2.铝的卤化物
离子型化合物 | AlF3 |
|
|
共价型化合物 | AlCl3 | AlBr3 | AlI3 |
共价型化合物的共同特点:熔点低,易挥发,易溶于有机溶剂,易形成双聚物。
无水AlCl3的水解反应非常剧烈并放出大量的热,甚至在潮湿的空气中也因强烈的水解而发烟。
3.铝的含氧酸盐
常见的铝的含氧酸盐有硫酸铝Al2(SO4)3,铝钾钒(明矾)KAl(SO4)2·12H2O等。
硫酸铝、硝酸铝溶于水后,由于Al3+的水解,溶液呈酸性。
![]()
铝的弱酸盐水解更加明显,甚至达到几乎完全的程度。
![]()
![]()
所以,弱酸的铝盐不能用湿法制得。
Al3+的鉴定:在氨碱性条件下,加入茜素,生成红色沉淀。
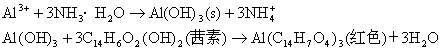
§12.4 p区元素化合物性质的递变规律
12.4.1 p区元素的氢化物
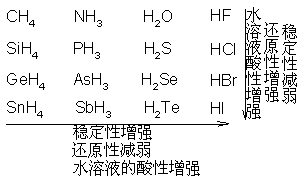
12.4.2 p区元素的氧化物及其水合物
1.氧化物
p区元素大多数都能与氧直接或间接地形成氧化物。稀有气体中只有氙能间接地与氧形成氧化物。同族元素同一氧化值的氧化物的酸碱性变化规律自上而下酸性逐渐减弱,碱性逐渐增强。
⒉氧化物水合物的酸碱性
同一周期p区元素最高氧化值氧化物的水合物从左到右碱性减弱,酸性增强。例如:
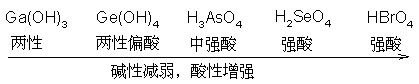
同族元素相同氧化值氧化物的水和物的酸碱性自上而下酸性减弱,碱性增强。
L·Pauling在研究含氧酸强度与结构之间的关系时,总结出下面的两条经验规则。
L·Pauling规则(定性)
★ 氢氧化物或含氧酸,可记作:(HO)mROn,其中m:羟基氧的个数;n:非羟基氧的个数。酸性的强弱取决于羟基氢的释放难易,而羟基氢的释放又取决于羟基氧的电子密度,若羟基氧的电子密度小,易释放氢,则酸性强。
★ 若中心原子R的电负性大,半径小,氧化值高则羟基氧的电子密度小,酸性强;非羟基氧的数目多,可使羟基氧上的电子密度减小,酸性增强。例如:
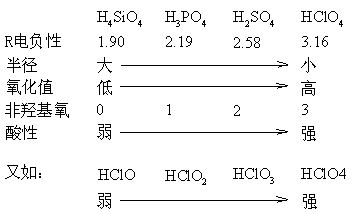
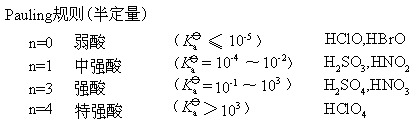
⒊ p区元素化合物的氧化还原性
对于同一元素不同氧化值的化合物来说,最高氧化值的化合物只可能有氧化性,且同一周期的最高氧化值化合物的氧化性从左到右依次增强。例如:
电对 | Al3+/Al | SiO2/Si | H3PO4/P |
|
|
| -1.68 | -0.9754 | 0.412 | 0.384 | 1.390 |
对于氯、溴、碘等非金属性较强的元素的不同氧化值的含氧酸来说,通常不稳定的酸氧化性较强。例如:
电对 |
|
| HClO2/Cl- | HClO/Cl- |
| 1.38 | 1.45 | 1.57 | 1.49 |
⒋ p区元素含氧酸的热稳定性
一般地说,含氧酸的热稳定性差,则相应的盐的热稳定性也较差。但是,含氧酸盐比相应的含氧酸要稳定些。
同一种含氧酸形成的盐,一般来说,金属越活泼,相应的含氧酸盐也越稳定。例如:
| Na2CO3 | BaCO3 | MgCO3 | FeCO3 | CdCO3 | Ag2CO3 |
分解温度/℃ | 1800 | 1360 | 540 | 280 | 345 | 275 |
1 / 29